
| A£® | øĆ·“Ó¦·Å³ö251.2 kJµÄČČĮæ | B£® | øĆ·“Ó¦ĪüŹÕ251.2 kJµÄČČĮæ | ||
| C£® | øĆ·“Ó¦·Å³ö125.6 kJµÄČČĮæ | D£® | øĆ·“Ó¦ĪüŹÕ125.6 kJµÄČČĮæ |
·ÖĪö ”÷H=·“Ó¦Īļ¼üÄÜŗĶ-Éś³ÉĪļ¼üÄÜŗĶ£¬¾Ż“Ė½ā“š£®
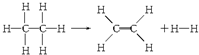
½ā“š ½ā£ŗ1molŅŅĶéŗ¬ÓŠ1molC-C¼ü£¬6molC-H¼ü£¬Éś³ÉµÄŅŅĻ©ŗ¬1molC=C¼ü1molH-H¼üŗĶ4molC-H¼ü£¬”÷H=347.4KJ+6”Į414.4KJ-4”Į414.4KJ-615.3KJ-435.3KJ=+125.6KJ£¬ĖłŅŌøĆ·“Ó¦ĪüŹÕ125.6KJµÄČČĮ棬
¹ŹŃ”£ŗD£®
µćĘĄ ±¾Ģāæ¼²éѧɜ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»ÆÖŖŹ¶£¬×¢Ņāøł¾Ż·“Ó¦ČČÓė¼üÄܵĹŲĻµ¼ĘĖć£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅŌŚĪŽÉ«ĶøĆ÷ĻøæŚĘæÖŠ | B£® | ÖĆÓŚĄä°µ“¦ | ||
| C£® | ÖĆÓŚĶØ·ēĶø¹ā“¦ | D£® | ¼ÓČėÉŁĮæMnO2»ņFeCl3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
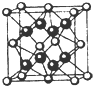 ŅŃÖŖA”¢B”¢C”¢DŗĶE¾łĪŖŌŖĖŲÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£®BŗĶCŠĪ³ÉµÄ-1¼ŪŅõĄė×Ó×īĶā²ć¾łĪŖ8µē×Ó£¬DŗĶEŹōĶ¬Ņ»ÖÜĘŚ£¬ÓÖÖŖEŹĒÖÜĘŚ±ķÖŠ1-18ĮŠÖŠµÄµŚ7ĮŠŌŖĖŲ£®DµÄŌ×ÓŠņŹż±ČEŠ”5£¬DøśBæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļĘ侧°ū½į¹¹ČēĶ¼£®Ēė»Ų“š£ŗ
ŅŃÖŖA”¢B”¢C”¢DŗĶE¾łĪŖŌŖĖŲÖÜĘŚ±ķÖŠĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£®AŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£®BŗĶCŠĪ³ÉµÄ-1¼ŪŅõĄė×Ó×īĶā²ć¾łĪŖ8µē×Ó£¬DŗĶEŹōĶ¬Ņ»ÖÜĘŚ£¬ÓÖÖŖEŹĒÖÜĘŚ±ķÖŠ1-18ĮŠÖŠµÄµŚ7ĮŠŌŖĖŲ£®DµÄŌ×ÓŠņŹż±ČEŠ”5£¬DøśBæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļĘ侧°ū½į¹¹ČēĶ¼£®Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
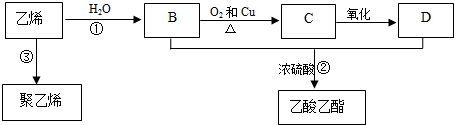
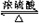 CH3COOC2H5+H2O£®
CH3COOC2H5+H2O£® +CaCl2+H2O
+CaCl2+H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £ØÓƵē×ÓŹ½±ķŹ¾£©£®
£ØÓƵē×ÓŹ½±ķŹ¾£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ż | B£® | ¢Ś¢Ü¢Ž | C£® | ¢Ż¢ß | D£® | ¢Ž¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
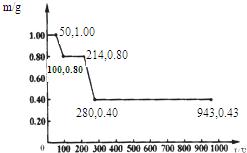 £Ø1£©ÓĆ¼×ĶéÖĘĒāŹĒŅ»ÖÖĮ®¼ŪµÄÖĘĒā·½·Ø£®ÓŠ¹ŲµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
£Ø1£©ÓĆ¼×ĶéÖĘĒāŹĒŅ»ÖÖĮ®¼ŪµÄÖĘĒā·½·Ø£®ÓŠ¹ŲµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øÖĢśÖĘĘ·±ķĆęĖ®Ä¤µÄĖįŠŌ½ĻĒæŹ±£¬Õż¼«µÄµē¼«·“Ó¦£ŗ2H++2e-ØTH2”ü | |
| B£® | ³£ĪĀĻĀ£¬ĀČ»Æļ§ČÜŅŗ³ŹĖįŠŌ£ŗNH4++OH-?NH3•H2O | |
| C£® | ĻņĮņĖįĆ¾ČÜŅŗÖŠ¼ÓČėBa£ØOH£©2ČÜŅŗ£¬½«ČÜŅŗÖŠµÄSO42-ĶźČ«³ĮµķĻĀĄ“£ŗSO42-+Ba2+ØTBaSO4”ż | |
| D£® | ĻņĀČ»ÆŅų×ĒŅŗÖŠ¼ÓČėĮņ»ÆÄĘČÜŅŗ²śÉśŗŚÉ«³Įµķ£ŗ2Ag++S2-ØTAg2S”ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com