
NA代表阿伏加德罗常数。下列有关叙述正确的是(Fe-56 O-16)( )
A.标准状况下,2.24LH2O含有的分子数等于0.1NA
B.5.6g Fe与足量稀盐酸反应,转移电子数为0.2 NA
C.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
D.18g重水(D2 O)所含的电子数为10NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014秋季甘肃省白银市高二第一学期期中理科化学试卷(解析版) 题型:选择题
在2A+B?3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol﹒L-1﹒s-1
B.v(B )=0.3 mol﹒L-1﹒s-1
C.v(C)=0.8 mol﹒L-1﹒s-1
D.v(D)=1.6 mol﹒L-1﹒min-1
查看答案和解析>>
科目:高中化学 来源:2014秋季湖南省高二上学期第一次阶段测试化学(B)试卷(解析版) 题型:选择题
对于密闭容器中进行的反应:2NO2  N2O4,下列说法正确的是
N2O4,下列说法正确的是
A.增大NO2的浓度,平衡常数增大
B.增大N2O4的浓度,平衡常数增大
C.增大NO2的浓度,正反应速率加快,逆反应速率减慢
D.增大NO2的浓度,平衡常数不变
查看答案和解析>>
科目:高中化学 来源:2014秋季湖南省高二上学期第一次阶段测试化学(B)试卷(解析版) 题型:选择题
.在溶液中发生的反应,对反应速率不发生影响的因素是
A.温度 B.压强 C.浓度 D.催化剂
查看答案和解析>>
科目:高中化学 来源:2015届广东省韶关市十校高三10月联考化学试卷(解析版) 题型:选择题
下一代iPhone将在电池方面有所改进,该电池的一极为一种有机高分子游离基(用R表示)和石墨粉及粘结剂的复合物,另一极是锂,分隔材料为某种聚烯烃,电解质为LiPF6溶解于某种有机碳酸酯溶剂中。该游离基(R)在空气中十分稳定,在充电时被氧化成阳离子(Rx+),电池充放电的方程式为:xLi+Rx+ xLi++R。下列有关说法正确的是( )
xLi++R。下列有关说法正确的是( )
A.放电时,该电池将电能转化为化学能
B.充电时,Rx+由阴极向阳极移动
C.放电时,负极反应为xLi-xe-=xLi+
D.充电时,阳极反应为R-xe-=Rx+
查看答案和解析>>
科目:高中化学 来源:2015届广东省肇庆市高三一模理综化学试卷(解析版) 题型:填空题
(16分)(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
① CH4(g)+H2O(g)=CO(g) + 3H2(g) △H =+206.0 kJ·mol-1
② CO(g)+2H2(g)=CH3OH (g) △H =-129.0 kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的△H= 。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为10 L的反应器,在一定条件下发生反应①,测得在一定压强下CH4的转化率与温度的关系如图。

假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为 mol·L-1·min-1。
(3)在某温度和压强下,将一定量 CO与H2充入密闭容器发生反应②生成甲醇,平衡后压缩容器体积至原来的l/2,其他条件不变,对平衡体系产生的影响是 (填序号):
A.c ( H2 )减少;
B.平衡常数K增大;
C.CH3OH 的物质的量增加;
D.正反应速率加快,逆反应速率减慢;
E.重新平衡c ( H2 )/ c (CH3OH )减小。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用图装置模拟上述过程,

则: Co2+在阳极的电极反应式为: ;除去甲醇的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省肇庆市高三一模理综化学试卷(解析版) 题型:选择题
下列各组离子能在水溶液中大量共存的是
A.H+、Fe2+、ClO-、SO42- B.Na+、Cu2+、S2-、ClO-
C.Na+、Ba2+、OH-、NO3- D.Na+、Al3+、SiO32-、CO32-
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:填空题
(16分)在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+ O2  2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。 SO2转化为SO3的热化学方程式是 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速率 。该反应K值将 。(填“增大”或“减小”或“不变”)
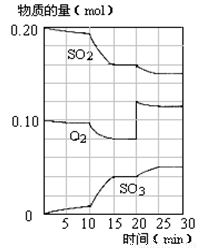
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.增大容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
鉴定NaCl的最佳方法是
A、焰色反应呈黄色,加硝酸酸化的AgNO3溶液有白色沉淀
B、焰色反应呈紫色,加盐酸酸化的AgNO3溶液有白色沉淀
C、焰色反应呈黄色,加盐酸酸化的AgNO3溶液有白色沉淀
D、焰色反应呈紫色,加硝酸酸化的AgNO3溶液有白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com