
| A. | 配制氯化铁溶液时需加入少量盐酸 | |
| B. | 金属钠保存在装有煤油的带玻璃塞的广口瓶中 | |
| C. | 保存液溴需用水封,放在带橡皮塞子的棕色细口瓶中 | |
| D. | 用稀硝酸洗去附在试管内壁的银镜 |
分析 A.氯化铁是强酸弱碱盐,铁离子易水解;
B.钠易和空气中水、氧气反应而变质,其密度大于没有且不和煤油反应;
C.溴易腐蚀橡皮塞;
D.银能溶于稀硝酸.
解答 解:A.氯化铁是强酸弱碱盐,铁离子易水解,为防止水解,在配制氯化铁溶液时需要加入少量稀盐酸,故A正确;
B.钠易和空气中水、氧气反应而变质,其密度大于没有且不和煤油反应,所以金属钠保存在装有煤油的带玻璃塞的广口瓶中,故B正确;
C.溴易腐蚀橡皮塞,应该用玻璃塞的试剂瓶,故C错误;
D.银能溶于稀硝酸生成硝酸银,所以可以用稀硝酸洗去附在试管内壁的银镜,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及盐类水解、药品贮存、物质性质等知识点,明确实验原理及物质性质是解本题关键,熟练掌握常见元素化合物性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
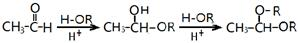

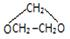 .
.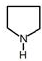 ,F
,F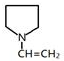 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若原料完全反应生成上述产物,CH2CH2Br与NH3的物质之比为2:1 | |
| B. | 该反应属于取代反应 | |
| C. | CH2CH2Br与HBr均属于电解质 | |
| D. | CH2CH2Br难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室配制480 mL 0.1 mol/L NaOH溶液,需要准确称量NaOH 1.920 g | |
| B. | 学生实验测定硫酸铜晶体中结晶水含量时,通常至少称量4次 | |
| C. | 酸碱中和滴定实验中只能用标准液滴定待测液 | |
| D. | 分液时,分液漏斗中下层液体从下口放出后,换一容器再从下口放出上层液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
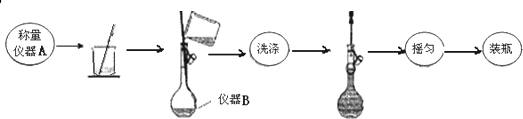

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
A、B、C、D、E、F、G、H八种主族元素分布在三个不同的短周期,它们在周期表中位置如下:
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
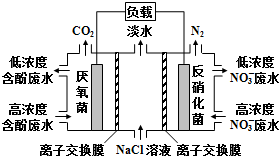
| A. | 右室电极为该电池的正极 | |
| B. | 左室电极反应式可表示为:C6H5OH-28e-+11H2O═6CO2↑+28H+ | |
| C. | 右室电极附近溶液的pH减小 | |
| D. | 工作时中间室的Cl-移向左室,Na+移向右室 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com