
 ,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;
,则V(C4H10):V(C2H4)=4:1,依此类推,故答案为:①C4H10、C3H6、3:2;②C4H10、C2H4、4:1③C4H10、C2H2、4:1④C4H10、C3H4、3:2;| 1 |
| 4 |
| 点燃 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 | ||
|
| ||
| 2L |


科目:高中化学 来源: 题型:
| A、离子化合物中可以含有共价键 |
| B、共价化合物中可以含有离子键 |
| C、当元素处于最高价态时一定具有强氧化性 |
| D、元素的性质呈周期性变化的根本原因是元素原子的核外电子排布呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间 | t1 | t2 | t3 | t4 | t5 |
| 剩余固体质量/g | 19.0 | 17.4 | 16.5 | 15.9 | 15.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
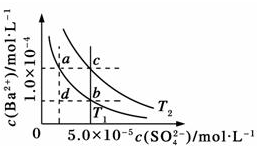
| A、T1>T2 |
| B、加入BaCl2固体,可使a点变成c点 |
| C、c点时,在T1、T2两个温度下均有固体析出 |
| D、a点和b点的Ksp相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、阳离子交换膜是A,不是B |
| B、通电后阳极区的电极反应式:2Cl--2e-→Cl2↑ |
| C、工业上阴极使用铁丝网代替石墨碳棒,以减少石墨的损耗 |
| D、阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com