
| A、Na2CO3溶液与NaHSO4溶液反应:CO32-+2H+=H2O+CO2↑ |
| B、向硫酸铵溶液中加入氢氧化钡溶液:Ba2+SO42-=BaSO4↓ |
| C、Fe3O4与稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O |
| D、少量金属钠加到冷水中:Na+2H2O=Na++OH-+H2↑ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池中失去电子的电极为正极 |
| B、在原电池的负极和电解池的阳极上都发生氧化反应 |
| C、原电池是将氧化还原反应产生的化学能转化为电能的一种装置 |
| D、电解的过程就是将电能转化为化学能的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、L、Q形成的简单离子核外电子数相等 |
| B、L、R的单质与盐酸反应速率为R>L |
| C、Q、T两元素的氢化物的稳定性为HnT<HnQ |
| D、M与T形成的化合物能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中的SO42-移向正极,一段时间后正极附近的SO42-浓度增大 |
| B、铜片是正极,锌片是负极 |
| C、正极吸收H2 |
| D、正极吸收O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、充电时,阴极反应(还原反应):6C+xLi++xe-═LixC6 |
| B、放电时,正极反应(还原反应)Li1-xCoO2+xLi++xe-═LiCoO2 |
| C、充电时,电池的负极与电源的负极相连 |
| D、放电时,Li+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
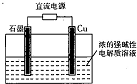 Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为:2Cu+H2O
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为:2Cu+H2O
| ||
| A、石墨电极上产生氢气 |
| B、铜电极发生的电极反应为:2Cu-2e-+2OH-?Cu2O+H2O |
| C、铜电极接直流电源的正极 |
| D、当有0.1mol电子转移时,有0.1mol Cu2O生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是由电能转化为化学能的装置 |
| B、原电池中电子流出的一极为负极,发生还原反应 |
| C、原电池中阳离子向负极移动 |
| D、原电池外电路中电流由正极流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com