
【题目】填空
(1)按要求完成下列问题:
① 甲基的电子式_________;
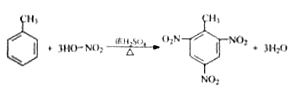
② 写出制备TNT的化学方程式__________;
③写出2-溴丙烷消去反应的化学方程式__________;
④ 写出实验室制乙炔的化学方程式__________;
⑤![]() 含有的官能团的名称为__________;
含有的官能团的名称为__________;
(2)某有机物的结构简式为 据此填写下列空格。
据此填写下列空格。
① 该物质苯环上一氯代物有__________;
② lmol该物质和溴水混合,消耗Br2的物质的量为__________mol;
③ lmol该物质和H2加成需H2__________mol。
(3)![]() 与一定量的Br2发生加成反应,生成的产物可能是_______。
与一定量的Br2发生加成反应,生成的产物可能是_______。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
(4)环蕃A(cyclophane)和超蕃B(superphane)是一种光电信息材料,都属于烃(B中氢原子未画出),它们的结构如图所示。

下列有关说法正确的是
A.环蕃和超蕃互为同系物 B.环蕃能使酸性高锰酸钾溶液褪色
C.环蕃能与液溴、硝酸发生取代反应 D.超蕃的一氯取代物只有l种,二氯取代物有3种
(5)实验证实,烯烃被酸性高锰酸钾溶液氧化时有如下规律:

己知某烃在通常情况下,只能跟等物质的量的溴反应:它与酸性高锰酸钾溶液反应时,所得氧化产物只有一种且没有支链,又知该烃充全燃烧时所需氧气的体积是相同悄况下烃蒸气的8.5倍,试分析该烃的结构简式________。
【答案】 ![]()
![]() CaC2+2H2O→Ca(OH)2+CH=CH↑ 碳碳三键 溴原子 4 5 B BC
CaC2+2H2O→Ca(OH)2+CH=CH↑ 碳碳三键 溴原子 4 5 B BC
【解析】(1)①甲基的化学式为-CH3,含有共价键,其电子式为![]() ;②甲苯和浓硝酸发生硝化反应得到TNT,反应的化学方程式为
;②甲苯和浓硝酸发生硝化反应得到TNT,反应的化学方程式为 ;③2-溴丙烷在氢氧化钠的醇溶液中加热发生消去反应的化学方程式为CH3CHBrCH3+NaOH
;③2-溴丙烷在氢氧化钠的醇溶液中加热发生消去反应的化学方程式为CH3CHBrCH3+NaOH![]() CH3CH=CH2↑+NaBr+H2O;④实验室制乙炔的化学方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;⑤
CH3CH=CH2↑+NaBr+H2O;④实验室制乙炔的化学方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;⑤![]() 含有的官能团的名称为碳碳三键和溴原子;(2)① 该物质苯环上的氢原子分为4类,其一氯代物有四种;②碳碳双键能与溴水发生加成反应,则lmol该物质和溴水混合,消耗Br2的物质的量为2mol;③苯环和碳碳双键均与氢气发生加成反应,lmol该物质和H2加成需H25mol。(3)二烯烃与溴加成时可以发生1,4-加成或1,2-加成或全加成,所以
含有的官能团的名称为碳碳三键和溴原子;(2)① 该物质苯环上的氢原子分为4类,其一氯代物有四种;②碳碳双键能与溴水发生加成反应,则lmol该物质和溴水混合,消耗Br2的物质的量为2mol;③苯环和碳碳双键均与氢气发生加成反应,lmol该物质和H2加成需H25mol。(3)二烯烃与溴加成时可以发生1,4-加成或1,2-加成或全加成,所以![]() 与一定量的Br2发生加成反应,生成的产物可能是
与一定量的Br2发生加成反应,生成的产物可能是![]() ,答案选B;(4)A.环蕃和超蕃所含碳原子数相同,不可能为同系物,A错误;B.环蕃中与苯环相连的碳上有氢原子,能使酸性高锰酸钾溶液褪色,B正确;C.环蕃中的H能被溴、硝基取代,C正确;D.超蕃的一氯取代物只有2种,D错误,答案选BC。(5)某烃在通常情况下只能跟等物质的量的溴反应,则含有1个碳碳双键双键,设烃的组成为CxHy,该烃完全燃烧时所需氧气的体积是相同情况下烃蒸气的8.5倍,则x+y/4=8.5,它与高锰酸钾酸性溶液反应时,所得到的氧化产物只有一种且没有支链,讨论可知x=6、y=10,则烃的分子式为C6H10,烃的不饱和度为2,还含有1个环,该烃的结构简式为
,答案选B;(4)A.环蕃和超蕃所含碳原子数相同,不可能为同系物,A错误;B.环蕃中与苯环相连的碳上有氢原子,能使酸性高锰酸钾溶液褪色,B正确;C.环蕃中的H能被溴、硝基取代,C正确;D.超蕃的一氯取代物只有2种,D错误,答案选BC。(5)某烃在通常情况下只能跟等物质的量的溴反应,则含有1个碳碳双键双键,设烃的组成为CxHy,该烃完全燃烧时所需氧气的体积是相同情况下烃蒸气的8.5倍,则x+y/4=8.5,它与高锰酸钾酸性溶液反应时,所得到的氧化产物只有一种且没有支链,讨论可知x=6、y=10,则烃的分子式为C6H10,烃的不饱和度为2,还含有1个环,该烃的结构简式为![]() 。
。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:
【题目】金属(M)﹣空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )

A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 在Mg﹣空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
C. M﹣空气电池放电过程的正极反应式:正极反应式为O2+2H2O+4e﹣=4OH﹣
D. 比较Mg、Al、Zn三种金属﹣空气电池,Mg﹣空气电池的理论比能量最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶1和1∶1分别形成两种化合物甲和乙。D、A按原子个数比3∶2形成化合物丙。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)B元素在周期表中的位置是___________________________。
(2)A、B、C、D、E五种元素的原子半径由大到小的顺序是(用元素符号填写)_______________。
(3)写出E的最高价氧化物对应的水化物分别与A、C两元素的最高价氧化物对应的水化物反应的离子方程式:①_____________________________________;
_____________________________________。
(4)D、A按原子个数比3∶2形成化合物丙的化学式为____________。
(5)C、B可按原子个数比1∶1形成化合物乙的电子式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物在日常生活、工业上有广泛的应用。
(1)铝原子核外有_____种不同运动状态的电子,有_____种能量不同的电子。
(2)氮化铝具有强度高,耐磨,抗腐蚀,熔点可达2200℃。推测氮化铝是______晶体,试比较组成该物质的两微粒半径大小____________________。
(3)可用铝和氧化钡反应可制备金属钡:2Al+4BaO![]() 3Ba↑+BaO·Al2O3的主要原因是 __________ (选填编号)。
3Ba↑+BaO·Al2O3的主要原因是 __________ (选填编号)。
a.Al活泼性大于Ba | b.Ba沸点比Al的低 | c.BaO·Al2O3比Al2O3稳定 |
(4)氢氧化铝在水中发生酸式电离的电离方程式为:____________________,
滴入少量盐酸,上述体系中Al3+浓度_______(填“增加”、“减少”或“不变”)。
(5)工业上用氢氧化铝、氢氟酸和碳酸钠制取冰晶石(Na3AlF6)。其反应物中有两种元素在周期表中位置相邻,可比较它们金属性或非金属性强弱的是_______ (选填编号)。
a.气态氢化物的稳定性
b.最高价氧化物对应水化物的酸(碱)性
c.单质与氢气反应的难易
d.单质与同浓度酸发生反应的快慢
(6)冰晶石可做电解氧化铝的助熔剂,此反应中若有0.6mol电子转移,则在________极可得金属铝的质量为__________克。工业上不用电解氯化铝而是用电解氧化铝的方法获得铝单质的原因_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧产生的SO2是引起酸雨的原因之一。
(1)每隔一定时间测定某处雨水样品的pH值:
![]()
雨水样品pH值变小的主要原因是____________________。
(2)反应2SO2(g)+O2(g)![]() 2SO3(g)+Q (Q>0),其化学平衡常数表达式_______;升高温度,K____________(填“变大”或者“变小”)。
2SO3(g)+Q (Q>0),其化学平衡常数表达式_______;升高温度,K____________(填“变大”或者“变小”)。
(3)判断已达到化学平衡状态的描述是______(选填编号)。
a.体系的压强不再发生变化 | b.2υ正(SO2)=υ逆(O2) |
c.c(SO2) = c(SO3) | d.气体总质量不再变化 |
(4)防治酸雨常用的措施:向煤中加石灰,减少 SO2的产生。这种煤燃烧后,大部分硫元素最终转化为固体盐是_____________。
(5)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看到浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因:_____________________。
(6)Na2SO3溶液呈碱性,可吸收尾气SO2。Na2SO3溶液呈碱性的原因(用离子方程式表示)_____________________;常温下,0.1mol/L该溶液中离子浓度由大到小排列___________(用离子符号表示)。
(7)常温下,NaHSO3溶液呈酸性,在Na2SO3溶液中滴加稀盐酸至中性时,溶质的主要成分有__________________。(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/ LNaOH溶液滴定25.00mL0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示。下列说法正确的是
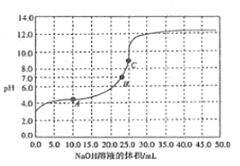
A. HX为强酸
B. 在A点,c(HX)>c(X-)>c(Na+)>c(H+)>c(OH-)
C. 在B点,两者恰好完全反应
D. 在C点.c(X-)+ c(HX)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的的是
A. 用溴水检验汽油中是否含有不饱和脂肪烃
B. 除去苯中混有的苯酚,加入浓溴水,过滤
C. 除去乙醇中混有的水,加入金属钠,蒸馏
D. 乙烷气体中混有乙烯, 通入酸性高锰酸钾溶液,洗气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com