
| A. | $\frac{2(a+b)}{5b}$×100% | B. | $\frac{a+b}{5b}$×100% | C. | $\frac{2(a+b)}{5}$×100% | D. | $\frac{2(a+b)}{5a}$×100% |
分析 设转化的Y为n,
X+2Y?2Z
开始 a b 0
转化 0.5n n n
平衡 a-0.5n b-n n
达到平衡时,n(X)+n(Y)=n(Z),则a-0.5n+b-n=n,解得n=$\frac{a+b}{2.5}$,以此来解答.
解答 解:设转化的Y为n,
X+2Y?2Z
开始 a b 0
转化 0.5n n n
平衡 a-0.5n b-n n
达到平衡时,n(X)+n(Y)=n(Z),则a-0.5n+b-n=n,解得n=$\frac{a+b}{2.5}$,
则Y的转化率为$\frac{\frac{a+b}{2.5}}{b}$×100%=$\frac{2(a+b)}{5b}$×100%,
故选A.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率的计算为解答的关键,侧重分析与应用能力的考查,注意平衡时物质的量关系,题目难度不大.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | a+b>c | B. | 平衡常数减小 | C. | Y的转化率增大 | D. | X的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=14的溶液中:Na+、CO32-、Al3+、ClO- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液中:K+、Fe2+、Cl-、SO42- | |
| C. | 加入铝片能放出H2的溶液中:Na+、HCO3-、Cu2+、SO42- | |
| D. | 水电离出来的c(H+)=10-13mol•L-1的溶液中:NH4+、K+、NO3-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体硫酸钡不能导电,所以硫酸钡是非电解质 | |
| B. | Cl2的水溶液能导电,所以Cl2是电解质 | |
| C. | NaOH溶液能导电,所以NaOH溶液是电解质 | |
| D. | CO2、SO2、SO3、NH3等均属于非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、空气、硝酸、干冰 | B. | 胆矾、漂白粉、氯化钾、硫酸钡 | ||
| C. | 蛋白质、油脂、烧碱、石灰石 | D. | 冰醋酸、海水、硫酸钠、乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑦ | B. | ③④⑤ | C. | ③⑤⑥ | D. | ③④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子体积的大小 | |
| B. | 分子间的间距变了分子间作用力的强弱变了 | |
| C. | 相对分子质量的大小 | |
| D. | 分子内共价键的长短 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )
利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )| A. | 该反应的△H<0,且p1<p2<p3 | |
| B. | 在C点时,H2转化率为75% | |
| C. | 反应速率:ν逆(状态A)>ν逆(状态B) | |
| D. | 在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,达平衡时CH3OH的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
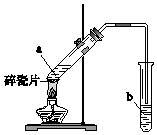 实验室用如图所示装置制备乙酸乙酯.
实验室用如图所示装置制备乙酸乙酯. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com