
(14分)工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号)__________
A. 生成CH3OH的速率与消耗CO的速率相等 B. 混合气体的密度不变
C. 混合气体的相对平均分子质量不变 D. CH3OH、CO、H2的浓度都不再发生变化
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①该反应化学平衡常数表达式K=
②由表中数据判断该反应的△H__________0(填“>”、“=”或“<”);
③某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得C(CO)=0.2mol·L-1,此时的温度为__________
(3)25℃101KPa下,1g液态甲醇完全燃烧生成CO2和液态水时放出热量22.68kJ,表示甲醇燃烧热的热化学方程式为
(4)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,该电池工作时负极电极反应式为 。若反应时消耗16g甲醇所产生的电能电解足量的CuSO4溶液,则将产生标准状况下的O2________升
⑴C、 D;⑵①K=c(CH3OH)/c(CO)·c2(H2) ; ②△H<0;③250℃
⑶ CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-725.76 kJ / mol
⑷ 负极CH3OH -6e-+8OH-=CO32-+6H2O ; 产生标准状况下的O216.8升
【解析】
试题分析:A. CH3OH是生成物,而CO是反应物,在任何时刻都存在生成CH3OH的速率与消耗CO的速率相等,因此不能作为判断平衡的标志。错误。B. 由于反应是在体积固定的密闭容器中进行,反应前后遵循质量守恒定律,所以在无论反应是否达到平衡,混合气体的密度都不变。因此不能作为判断平衡的标志。错误。C. 由于该反应是个反应前后气体体积不等的可逆反应,若未达到平衡,气体的物质的量就要发生变化,则气体的密度也要发生变化,即混合气体的相对平均分子质量也要发生变化。因此混合气体的相对平均分子质量不变。可以作为判断反应达到平衡的标志。正确。D. 若反应达到平衡,反应混合物中CH3OH、CO、H2的任何一个组分的消耗浓度与产生浓度相等,即浓度都不再发生变化。因此可以作为判断反应达到平衡的标志。正确。⑵ ①化学平衡常数是可能反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数的乘积的比。所以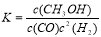 。②由表中数据可知:升高温度,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度化学平衡向吸热反应方向移动。逆反应方向为吸热反应方向,所以该反应的正反应为放热反应,△H<0。③CO(g)+2H2(g)
。②由表中数据可知:升高温度,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度化学平衡向吸热反应方向移动。逆反应方向为吸热反应方向,所以该反应的正反应为放热反应,△H<0。③CO(g)+2H2(g) CH3OH(g)在反应开始时c(CO)=1mol/L;c(H2)=3mol/L;c(CH3OH)=0mol/L;当反应达到平衡时,C(CO)=0.2mol/L,所以根据方程式中各种物质的关系可知c(H2)=1.4mol/L;c(CH3OH)= 0.8mol/L化学平衡常数
CH3OH(g)在反应开始时c(CO)=1mol/L;c(H2)=3mol/L;c(CH3OH)=0mol/L;当反应达到平衡时,C(CO)=0.2mol/L,所以根据方程式中各种物质的关系可知c(H2)=1.4mol/L;c(CH3OH)= 0.8mol/L化学平衡常数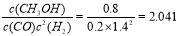 所以反应温度为250℃。(3)燃烧热是1mol的物质完全燃烧产生稳定的氧化物时放出的热量。根据题目提供的数据可知:表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-725.76 kJ / mol;(4)在燃料电池中,通入燃料的电极为负极,通入氧气的电极为正极。由于电解质为碱性,所以在负极的电极反应式为CH3OH -6e-+8OH-=CO32-+6H2O。n(CH3OH)=16g÷32g/mol=0.5mol.所以n(e-)=0.5mol×6=3mol.根据电子守恒可得n(O2)=3mol÷4=0.75mol,V(O2)= 0.75mol×22.4L/mol=16.8L。
所以反应温度为250℃。(3)燃烧热是1mol的物质完全燃烧产生稳定的氧化物时放出的热量。根据题目提供的数据可知:表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-725.76 kJ / mol;(4)在燃料电池中,通入燃料的电极为负极,通入氧气的电极为正极。由于电解质为碱性,所以在负极的电极反应式为CH3OH -6e-+8OH-=CO32-+6H2O。n(CH3OH)=16g÷32g/mol=0.5mol.所以n(e-)=0.5mol×6=3mol.根据电子守恒可得n(O2)=3mol÷4=0.75mol,V(O2)= 0.75mol×22.4L/mol=16.8L。
考点:考查化学平衡状态的判断、化学平衡常数的表达及计算、燃料电池的电极式、及相应的计算的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014四川省成都市高三第三次诊断性考试理综化学试卷(解析版) 题型:选择题
常温下,下列指定条件下能大量共存的微粒是
A、乙醇稀溶液:K+、Na+、SO42—、OH—
B、氨水溶液:Mg2+、Ag+、NO3—、CH3COOH
C、c(OH—)/c(H+)=1012溶液:H2S、Ca2+、Ba2+、HCO3—
D、使石蕊变红的溶液:Fe2+、Al3+、ClO—、CO32—
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高二下学期期中联考化学试卷(解析版) 题型:选择题
有关下列叙述不正确的是
A.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
B.干馏煤可以得到甲烷、苯和氨等重要化工原料
C.用于奥运“祥云”火炬的丙烷是一种清洁燃料
D.油脂的皂化反应生成高级脂肪酸钠和丙三醇
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高一下学期期中联考化学试卷(解析版) 题型:选择题
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
A、离子半径:C>D>B>A B、原子序数:d>c>b>a
C、原子半径:A>B>C>D D、单质的还原性:A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列各分子中所有原子都满足最外层为8电子结构的是( )
A、BeCl2 B、BF3 C、PCl5 D、CCl4
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
DDT是人类合成得到的第一种有机农药,它的结构简式如下图所示,有关它的说法正确的是
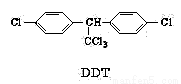
A.它属于芳香烃
B.分子式为C14H8Cl5
C.1mol该物质能与6mol H2加成
D.分子中最多可能有27个原子共面
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省宜昌市春季期中考试高二化学试卷(解析版) 题型:选择题
下列分子中,各原子均处于同一平面上的是
A.NH3 B.CCl4 C.SO32- D.CH2O
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省高三5月冲刺卷理综化学试卷(解析版) 题型:推断题
(15分)有机物E与铜(Ⅱ)的配合物是一种可发光的发光材料,在发光器材方面有很好的应用前景。其合成E的路线如下:
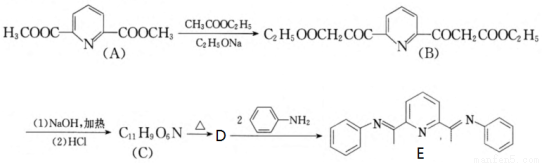
回答下列问题:
(1)B生C的反应类型有 。
(2)A有多种同分异构体,其中符合以下条件的共有 种。
①分子中含有吡啶环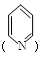 且环上只有2个取代基;
且环上只有2个取代基;
②只含有一种官能团,且核磁共振氢谱只有四种峰;
③吡啶环上的一氯取代物只有2种。
(3)C生成D的过程中有一种温室气体生成,则D的结构简式为 。
(4)写出D生成E的化学方程式 。
(5)结合题给信息,以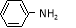 和
和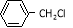 为原料合成西佛碱N-苯基苯甲亚胺(
为原料合成西佛碱N-苯基苯甲亚胺(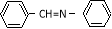 ),请你拟出合成路线: 。
),请你拟出合成路线: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省长春市高一下学期期末考试化学试卷(解析版) 题型:填空题
(共6分)一定温度下,在一定容积的密闭容器中发生如下可逆反应:
2A(g)+B(g) 2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
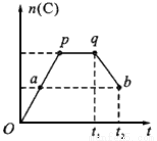
(1)a点时,反应的v(正) v(逆)(填“>”、“<”或“=”);
(2)此反应的逆反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率:v(a) v(b)
(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com