
下列各种基态原子的核外电子排布式中,正确的是( )
A.1s22s12p2 B.1s22s22p33s1
C.1s22s22p63s14s1 D.1s22s22p63s23p64s1
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)在常温常压下,32 g 18O2中含有2NA氧原子( )
(2)17 g —OH与17 g OH-所含电子数均为10NA( )
(3)相同质量的N2O4与NO2中所含原子数目相同( )
(4)m g CO与N2的混合气体中所含分子数目为 NA( )
NA( )
(5)4.5 g SiO2晶体中含有的硅氧键的数目为0.3NA( )
(6)30 g甲醛中含共用电子对总数为4NA( )
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需要配制0.50 mol·L-1 NaCl溶液480 mL。
按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为5 g)、药匙、烧杯、______、______、________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体______ g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是________________________________________________________________________
________________________________________________________________________。
(5)转移、洗涤。在转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了________________________________________________________________________。
(6)定容。向容量瓶中加水至液面接近刻度线________处,改用________加水,使溶液凹液面与刻度线相切。
(7)摇匀、装瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
按能量由低到高的顺序排列正确的一组是( )
A.1s、2p、3d、4s B.1s、2s、3s、2p
C.2s、2p、3s、3p D.4p、3d、4s、3p
查看答案和解析>>
科目:高中化学 来源: 题型:
日常生活中广泛应用的不锈钢,在其生成过程中添加了铬等元素。已知铬的原子序数为24,则它的价电子排布式为( )
A.3d44s2 B.3d104s1 C.3d54s1 D.3d64s0
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素原子序数为33,则
(1)此元素原子的电子总数是________,有________个未成对电子。
(2)有________个电子层,________个能级,________个原子轨道。
(3)它的价电子排布式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜,制备方法如下:
方法一
(1)浓硫酸试剂瓶上适合贴上的标签是________(填序号)。
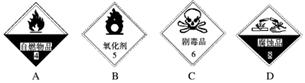
(2)甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分,设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:________________________________________________________。
实验结论:所得灰白色固体的化学式为__________。
(3)乙还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是(用化学方程式回答)_____________________________ _____________________________________。
直到最后反应完毕,发现试管中还有铜片剩余,乙根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是______________________________________。
方法二
(4)丙同学认为甲设计的实验方案不好,他自己设计的思路是2Cu+O2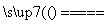 2CuO,CuO+H2SO4===CuSO4+H2O。
2CuO,CuO+H2SO4===CuSO4+H2O。
对比甲的方案,你认为丙同学的优点是
①________________________________________________________________________;
②________________________________________________________________________。
方法三
(5)丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水发现溶液逐渐呈蓝色,写出反应的化学方程式_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com