
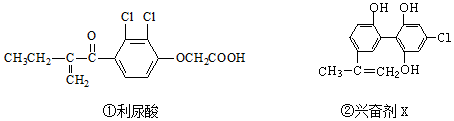
| A. | 两种分子均属于烃类 | |
| B. | 两种分子中均有相同的官能团 | |
| C. | 两种分子中的所有碳原子均不可能共平面 | |
| D. | 两种兴奋剂均能发生取代反应 |
分析 A、二者结构中含有卤原子、氧原子,烃是只含有碳氢两种元素的化合物;
B、利尿酸中含有羰基、卤原子、碳碳双键、醚基和羧基;兴奋剂中含羟基、卤原子、碳碳双键;
C、根据甲烷、乙烯和苯的结构判断两种分子中碳原子是否共面;
D、苯环、羧基、羟基等基团可以发生取代反应.
解答 解:A、烃是只含有碳氢两种元素的化合物,利尿酸和兴奋剂X中都含有卤原子、氧原子,不属于烃类,故A错误;
B、利尿酸中含有羰基、卤原子、碳碳双键、醚基和羧基;兴奋剂中含羟基、卤原子、碳碳双键,官能团不同,故B错误;
C、利尿酸中含有亚甲基,所以所有碳原子不可能共平面;乙烯是平面结构,兴奋剂X中相当于乙烯分子中的氢原子被苯环取代,苯环上所有碳原子共面,所以兴奋剂X中所有碳原子共平面,故C错误;
D、两种有机物中的苯环、羧基、羟基等基团可以发生取代反应,故D正确.
故选D.
点评 本题考查了有机物的结构和性质,根据甲烷、乙烯和苯的结构确定这两种分子中碳原子是否共面即可.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.01 mol•L-1的蔗糖溶液 | B. | 0.01 mol•L-1的CaCl2溶液 | ||
| C. | 0.02 mol•L-1的NaCl溶液 | D. | 0.02 mol•L-1的CH3COOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色一氧化氮气体与空气接触变为红棕色 | |
| B. | 往盐酸中滴加紫色石蕊试液,溶液变红色 | |
| C. | 向硫酸铜溶液中滴加氢氧化钠溶液,出现白色沉淀 | |
| D. | 将足量二氧化硫气体通入品红溶液,红色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol OH-含有7NA个电子 | |
| B. | 0.012kg碳中所含有的碳原子数为NA | |
| C. | 10g46%的乙醇溶液含O数为0.4NA | |
| D. | 0.5mol/L碳酸钠中含有的Na+为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
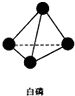 ,并指出1mol白磷(P4)含有P-P键的数目6NA
,并指出1mol白磷(P4)含有P-P键的数目6NA查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(Fe)=0.5 mol•L-1•min-1 | B. | v(H2SO4)=1 mol•L-1•min-1 | ||
| C. | v(H2)=0.05 mol•L-1•min-1 | D. | v(FeSO4)=0.5 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
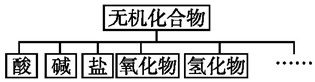
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com