
分析 (1)碳酸钠和碳酸氢钠的固体混合物,与盐酸溶液恰好完全反应,得到单一的氯化钠固体,根据氯守恒分析解答;
(2)设碳酸钠和碳酸氢钠的固体混合物中两者的物质的量分别为xmol和ymol,则:$\left\{\begin{array}{l}{106x+84y=19.0g}\\{2x+y=0.3}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.1mol}\\{y=0.1mol}\end{array}\right.$,根据碳守恒,求二氧化碳的物质的量,然后求体积.
解答 解:(1)150mL1.0mol/L盐酸的物质的量为:0.150L×1.0mol/L=0.15mol,所以氯化钠的物质的量为0.15mol×2=0.3mol,则该混合固体中含有Na+ 0.3mol,故答案为:0.3;
(2)设碳酸钠和碳酸氢钠的固体混合物中两者的物质的量分别为xmol和ymol,则:$\left\{\begin{array}{l}{106x+84y=19.0g}\\{2x+y=0.3}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.1mol}\\{y=0.1mol}\end{array}\right.$,根据碳守恒,所以二氧化碳的物质的量为0.1+0.1=0.2mol,所以体积为:0.2mol×22.4L/mol=4.48L,故答案为:4.48.
点评 本题考查根据方程式的有关计算以及守恒知识在解题中的应用等,难度不大,根据所学知识即可完成.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
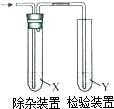 用下列方法制备乙烯,并用右图装置检验乙烯,不需要除杂的是( )
用下列方法制备乙烯,并用右图装置检验乙烯,不需要除杂的是( )| 乙烯的制备 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
| C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的水溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维的主要成分是二氧化硅 | |
| B. | 水玻璃是硅酸钠的俗称 | |
| C. | 单质硅是一种重要的半导体材料 | |
| D. | 二氧化硅能与氧化钙反应生成一种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
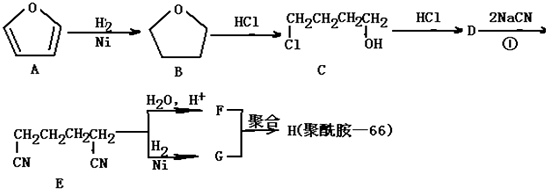
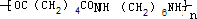 H+(2n-1)H2O.
H+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
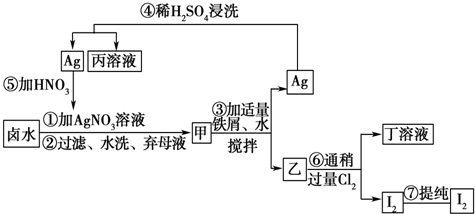
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同周期的IA族元素的金属性比IIA族的元素金属性强 | |
| B. | 第三周期元素的阴离子半径从左到右逐渐减小 | |
| C. | VIA族的气态氢化物一定比VA族的稳定性强 | |
| D. | 原子晶体的熔点一定比离子晶体的高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>②>①>④ | B. | ②>③>④>① | C. | ②>③>①>④ | D. | ①>③>④>② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com