
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
 |
0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol?L-1 | 0.100 | a | 0.5b | 0.4b | ||
| c(NO2)/mol?L-1 | 0 | 0.060 | b | c1 | c2 | c3 |
| c(H2SiO4) |
| c(SiO2).c2(H2O) |
| c(H2SiO4) |
| c(SiO2).c2(H2O) |
查看答案和解析>>
科目:高中化学 来源:2008届宁夏银川一中高三年级第六次月考测试、理科综合试卷化学部分 题型:022
将1 mol I2(g)和2 mol H2(g)置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)![]() 2HI(g);ΔH<0,并达到平衡.HI的体积分数Φ(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g);ΔH<0,并达到平衡.HI的体积分数Φ(HI)随时间变化如图曲线(Ⅱ)所示:

(1)达平衡时,I2(g)的物质的量浓度为________mol·L-1.
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线
(Ⅰ)所示,则该条件可能是________(填入下列条件的序号).
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2 L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应达平衡时,HI的体积分数仍为0.60,则a、b、c的关系为________(用一个含a、b、c的代数式表示).
(4)室温时将0.01 mol HI气体溶于水配成100 ml溶液,则该溶液中由水电离产生的氢离子的物质的量浓度为________mol·L-1;若降低温度该溶液的pH值将________(填增大、减小或不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
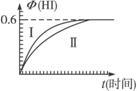
(1)达平衡时,I2(g)的物质的量浓度为______________mol·L-1。
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线(Ⅰ)所示,则该条件可能是_________________(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2 L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应达平衡时,HI的体积分数仍为0.60,则a、b、c的关系为______________(用一个含a、b、c的代数式表示)。
(4)室温时将0.01 mol HI气体溶于水配成100 ml 溶液,则该溶液中由水电离产生的氢离子的物质的量浓度为____________mol·L-1;若降低温度该溶液的pH将____________(填增大、减小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将1mol I2(g)和2mol H2(g)置于某2L密闭容器中,在一定温度下发生反应:
I2(g)+H2(g)![]() 2HI(g); ΔH<0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图曲线(II)所示:
2HI(g); ΔH<0,并达到平衡。HI的体积分数Φ(HI)随时间变化如图曲线(II)所示:
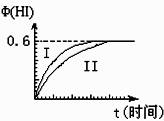
(1)达平衡时,I2(g)的物质的量浓度为 mol?L-1。
(2)若改变反应条件,在某条件下Φ(HI)的变化如曲线
(I)所示,则该条件可能是 (填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温、恒容条件下,加入适当催化剂
(3)若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2(g)和c mol HI(g)(a、b、c均大于0),发生反应达平衡时,HI的体积分数仍为0.60,则a、b、c的关系为 (用一个含a、b、c的代数式表示)。
(4)室温时将0.01 mol HI气体溶于水配成100 ml溶液,则该溶液中由水电离产生的氢离子的物质的量浓度为 mol?L-1 ;若降低温度该溶液的pH值将 (填增大、减小或不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com