
正误判断,正确的打“√”,错误的打“×”
(1)所有的燃烧反应都是放热反应,所以不需要加热就能进行( )
(2)反应物的总能量低于生成物的总能量时,一定不能发生反应( )
(3)物理变化过程中,也可能有热量的变化( )
(4)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
(5)一个反应的焓变因反应物的用量和反应条件的改变而发生改变( )
(6)催化剂能改变反应的焓变( )
(7)已知S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ·mol-1,则S(s)+O2(g)===SO2(g)反应放出的热量大于293.23 kJ·mol-1( )
(8)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH不同( )
 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
有下列几个变化:①Na2CO3→Na2SiO3,②SiO2→H2SiO3;③Na2SiO3 →Na2 CO3;④
CO3;④
Ca(NO3)2→CaSiO3,其中不能通过一步反应实现的是 ( )
A.①② B.②④ C.③④ D.只有②
查看答案和解析>>
科目:高中化学 来源: 题型:
菱锰矿的主要成分是MnCO3(含有少量FeS2、Al2O3),以菱锰矿为原料制备锰单质的流程如下所示:

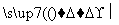 浆化
浆化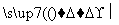 溶液1
溶液1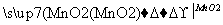 溶液2
溶液2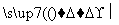 精制—→电解—→Mn
精制—→电解—→Mn
请回答下列问题:
(1)菱锰矿在浸取前需要粉碎,其目的是______________________________。
(2)用稀硫酸浸取时,主要反应的离子方程式为____________;加入二氧化锰时被氧化的物质是____________(填化学式)。
(3)已知Fe、Al、Mn的氢氧化物开始沉淀及沉淀完全时的pH如表所示,则加氨水沉淀时应控制溶液的pH范围为______________。此时得到的沉淀是____________、__________(填化学式)。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀pH | 1.8 | 4.1 | 8.3 |
| 完全沉淀pH | 3.2 | 5.0 | 9.8 |
(4)电解硫酸锰溶液时,阴极的电极反应式为____________________。用酸性高锰酸钾溶液检验Mn2+,产生黑色沉淀,该反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下纯水的pH=6。
(1)pH=7的溶液呈__________(填“酸性”“中性”或“碱性”);
(2)该温度下0.1 mol·L-1的盐酸溶液的pH=__________;
(3)0.05 mol·L-1的Ba(OH)2溶液的pH=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是一种极弱的电解质,在常温下平均每n个水分子只有1个分子发生电离,n的值是( )
A.1×1014 B.55.6×107
C.1×107 D.55.6
查看答案和解析>>
科目:高中化学 来源: 题型:
C、H2、CH4都是优质的能源物质,目前对这三种物质的研究是燃料研究的重点,下列关于这三种物质的研究方向中可行的是( )
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2,并放出热量
B.寻找优质催化剂,在常温常压下使CO2分解生成碳与O2
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
D.将固态碳合成为C60,以C60作为燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
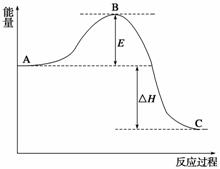
请回答下列问题:
(1)图中A、C分别表示__________、__________,E的大小对该反应的反应热有无影响?__________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________,理由是_________________________________________________________;
(2)图中ΔH=__________kJ·mol-1;
(3)V2O5的催化循环机理可能为V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:________________________________________________________________________;
(4)已知常温下,1 mol固体硫燃烧生成二氧化硫气体时放出的热量是296 kJ,计算由S(s)生成3 mol SO3(g)的ΔH________(要求写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求回答下列问题:
(1)已知:4Al(s)+3O2(g)===2Al2O3(s)
ΔH=-2 834.9 kJ·mol-1①
Fe2O3(s)+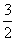 C(s)===
C(s)===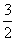 CO2(g)+2Fe(s)
CO2(g)+2Fe(s)
ΔH=+234.1 kJ·mol-1②
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1③
写出铝与氧化铁发生铝热反应的热化学方程式________________________________________________________________________。
(2)已知:
N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ·mol-1①
N2(g)+3H2(g)===2NH3(g)
ΔH=-92.4 kJ·mol-1②
2H2(g)+O2(g)===2H2O(g)
ΔH=-483.6 kJ·mol-1③
若有17 g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C10H14,属于苯的同系物,且苯环上的一氯代物只有2种的有机物有(不考虑立体异构,苯环上至少有3个氢)
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com