
 铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将铁与一定量的浓硫酸加热时,观察到铁完全溶解得到溶液A,并产生大量气体B.
铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将铁与一定量的浓硫酸加热时,观察到铁完全溶解得到溶液A,并产生大量气体B.| 实验操作 | 预期现象 | 结 论 | |
| 验证猜想Ⅰ | ①取适量A溶液,滴加0.1mol/LKSCN溶液 ②另取适量A溶液,滴加少量0.01mol/L酸性KMnO4溶液 | ①酸性高锰酸钾溶液褪色,说明含有亚铁离子; ②溶液变为血红色 | 含有Fe2+和Fe3+ |
| 验证猜想Ⅱ | 将所得气体通入下图所示装置 | 甲中紫色褪去,乙中不褪色,试管中收集到气体 | 含有两种气体 |
分析 【提出猜想】铁和浓硫酸反应生成二氧化硫或氢气或二者都有;
【实验探究】根据仪器作用选取仪器,注意填的是玻璃仪器;
验证猜想I:亚铁离子能使酸性高锰酸钾溶液褪色,铁离子能使KSCN溶液变红色;
验证猜想II:二氧化硫能使酸性高锰酸钾溶液褪色,氢气不溶于水,利用排水法能收集到氢气;
【问题讨论】装置乙的作用是证明二氧化硫已经除尽,二氧化硫能够使品红溶液褪色,故也可使用品红溶液.
解答 解:【提出猜想】浓硫酸和铁反应生成二氧化硫,稀硫酸和铁反应生成氢气,所以所得气体中可能含有SO2、H2,
故答案为:SO2、H2中的一种或两种;
【实验探究】配制过程中,用托盘天平称量高锰酸钾、用胶头滴管定容,所以还需要的玻璃仪器为胶头滴管;
验证猜想I:亚铁离子能使酸性高锰酸钾溶液褪色,铁离子能使KSCN溶液变红色,其检验方法为:取少量液体倒入试管中,向试管中滴加KSCN溶液后,溶液变为血红色,说明含有铁离子,向溶液中滴加酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,说明含有亚铁离子,如果两种现象都有,则说明含有铁离子和亚铁离子;
验证猜想II:二氧化硫有还原性,能和强氧化性的物质发生氧化还原反应,如能使酸性高锰酸钾溶液褪色,氢气不能使酸性高锰酸钾溶液褪色,但氢气不易溶于水,所以如果甲中KMnO4溶液褪色,说明含有二氧化硫;乙中KMnO4溶液颜色不变,说明二氧化硫完全被吸收,如果试管中收集气体,只能是氢气,
故答案为:胶头滴管;
| 实验操作 | 预期现象 | 结论 | |
| 验证猜想Ⅰ | ①取适量A溶液,滴加0.1 mol/L KSCN溶液 ②另取适量A溶液,滴加少量0.01 mol/L酸性KMnO4溶液 | ①酸性高锰酸钾溶液褪色,说明含有亚铁离子;②溶液变为血红色 | |
| 验证猜想Ⅱ | 甲中紫色褪去,乙中不褪色,试管中收集到气体 |
点评 本题考查了浓硫酸的性质、性质实验方案设计,题目难度中等,明确物质的性质为解答关键,根据物质的性质确定可能发生的反应及反应现象,注意掌握亚铁离子及铁离子的检验方法、性质实验方案的设计原则.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 除③外 | B. | 除①④⑥外 | C. | 除②③⑤外 | D. | 除②⑤外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体系压强不变 | |
| B. | 单位时间消耗n molA,同时生成2nmolC | |
| C. | 容器内气体密度不变 | |
| D. | A、B、C、D的反应速率之比为1:1:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20℃,20mL、3mol/L的Na2S2O3溶液 | B. | 10℃,10mL、4mol/L的Na2S2O3溶液 | ||
| C. | 10℃,30mL、2mol/L的Na2S2O3溶液 | D. | 20℃,10mL、4mol/L的Na2S2O3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )| A. | 该反应在0~8 min内CO2的平均反应速率是 0.375 mol•L-1•min-1 | |
| B. | 若起始时向上述容器中充入3 mol CO2和4 mol H2,则平衡时H2的体积分数大于20% | |
| C. | 若起始时向上述容器中充入4 mol CO2、2 mol H2、2 mol CH3OH和1mol H2O(g),则此时反应向正反应方向进行 | |
| D. | 改变条件得到曲线Ⅱ、Ⅲ,则曲线Ⅱ、Ⅲ改变的条件分别是升高温度、充入氦气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
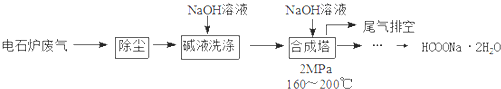
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
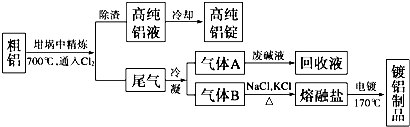
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
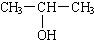 的方法是( )
的方法是( )| A. | 加入金属钠 | |
| B. | 加银氨溶液 | |
| C. | 在铜存在下和氧气反应 | |
| D. | 在铜存在下和氧气反应后的产物中加入银氨溶液共热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com