
| A. | 氯水中:c(Cl2)═2[c(ClO-)+c(Cl-)+C(HClO)] | |
| B. | 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) | |
| C. | 等体积等浓度的氢氧化钠与醋酸混合:c(Na+)>c(CH3COO-) | |
| D. | Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
分析 A.氯水中存在物料守恒,氯气中氯元素守恒;
B.氯水中氢离子浓度大于氯离子;
C.等体积等浓度的氢氧化钠与醋酸混合生成醋酸钠溶液,醋酸根离子水解溶液显碱性;
D.Na2CO3溶液中碳酸根离子分步水解溶液显碱性.
解答 解:A.氯水中存在物料守恒,c(Cl2)═2[c(ClO-)+c(Cl-)+C(HClO)],故A正确;
B.氯水中发生反应的离子方程式:Cl2+H2O=H++Cl-+HClO,存在水的电离平衡,溶液中c(Cl-)<c(H+),故B错误;
C.等体积等浓度的氢氧化钠与醋酸混合生成醋酸钠溶液,醋酸根离子水解溶液显碱性,c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C正确;
D.Na2CO3溶液中碳酸根离子分步水解溶液显碱性,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故D正确.
故选B.
点评 本题考查了盐类水解、电解质溶液中电荷守恒、物料守恒、离子浓度大小比较,注意微粒间的大小判断,掌握基础是解题关键,题目难度中等.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲酸乙酯 | B. | 乙酸甲酯 | C. | 乙酸丙酯 | D. | 丙酸丁酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
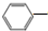 CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$
CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$ CHCl-CH3(g)+HCl(g)△H>0
CHCl-CH3(g)+HCl(g)△H>0| 时间/(min) | 0 | 2 | 5 | 6 | 9 | 10 |
| χ(乙苯) | 0.5 | 0.25 | 0.1 | 0.1 | 0.05 | 0.05 |
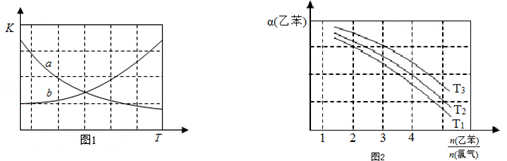
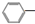 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)△H=+124kJ/mol
CH=CH2(g)+H2(g)△H=+124kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
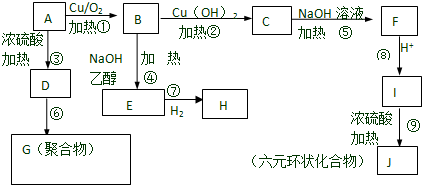
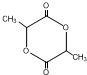 ;
;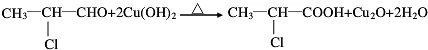 C→F
C→F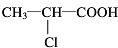 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$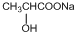 +NaCl+H2O
+NaCl+H2O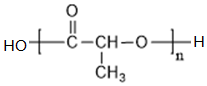 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素的最高正化合价依次升高 | |
| C. | B、C、N、O、F原子半径依次增大 | |
| D. | Li、Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
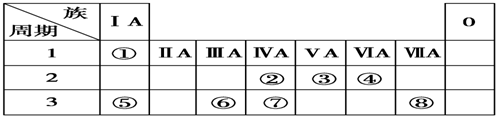
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com