
【题目】下列说法正确的是
A.只含有一种元素的物质一定是纯净物
B.含有共价键的化合物一定是共价化合物
C.石墨转变为金刚石为化学变化
D.水很稳定是因为水分子间存在较强的分子间作用力
科目:高中化学 来源: 题型:
【题目】化学与生活、生产和社会发展密切相关。下列说法正确的是
A. 《天工开物》中“凡石灰,经火焚炼而用”里的石灰,指的是Ca(OH)2
B. 某品牌的八宝粥不含任何糖类物质,糖尿病人可以放心食用
C. 未成熟的苹果肉遇碘酒变蓝,成熟苹果的汁液不能与银氨溶液反应
D. 用氯化铁溶液洗涤银镜反应后的试管比用硫酸铁溶液效果好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g。
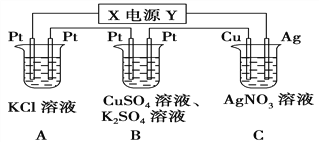
(1)电源电极X的名称为________;
(2)A中发生的离子方程式为_______________________
(3)B中阳极的电极反应式为___________________________
(4)pH变化:A_______,B_______,C_______。(填“增大”“减小”或“不变”)
(5)通电5 min后,B中共收集224 mL气体(标准状况),溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为______________(设电解前后溶液体积无变化)。
(6)若A中KCl溶液的体积也是200 mL,电解后,溶液的pH为_______(设电解前后溶液体积无变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3Fe(A2B4)3·3H2O(M)是制备负载型活性铁催化制的主要原料,也是一些有机反应催化剂,因而具有工业生产价值。A、B均为常见短周期非金属元素。某研究小组将纯净的化合物M在一定条件下加热分解,对所得气体产物有固体产物的组成进行探究。
(1)经实验分析,所得气体产物由甲、乙和水蒸气组成。甲、乙均只含A、B两种元素,甲能使澄清的石灰水交浑浊,乙常用于工业炼铁。
①写出甲的电子式:_________。
②写出工业炼铁的化学反应方程式:_______________。
(2)该研究小组查阅资料后推知,固体产物中不存在+3价铁,盐也只有K2AB3。小组同学对固体产物进行进行如图所示定量分析。

①操作I的具体操作为____________;“固体增重”说明固体产物中定含有的物质的化学式为_____________。
②写出与酸性KMnO4溶液反府的金属阳离子的离子结构示意图:_____________;用酸性KMnO4溶液去滴定该溶液时,终点颜色变化为______________。
③已知在酸州条件下KMnO4的还原产物为Mn2+,以上实验数据分析计算固体产物中各物质及它们之间的物质的量之比为_____________。
(3)写出复盐M加热分解的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2、NO、CO、NO2-等是常见大气污染物和水污染物,研究NO2、NO、CO、NO2-等的处理对建设美丽中国具有重要意义。
已知:①NO2+CO![]() CO2+NO,该反应的平衡常数为K1(下同)。断开1mol下列物质的所有化学键时所消耗能量分别为:
CO2+NO,该反应的平衡常数为K1(下同)。断开1mol下列物质的所有化学键时所消耗能量分别为:
NO2 | CO | CO2 | NO |
812kJ | 1076kJ | 1490kJ | 632kJ |
②![]() N2(g)+
N2(g)+ ![]() O2(g)
O2(g)![]() NO(g) △H=+89.75kJ/mol,K2
NO(g) △H=+89.75kJ/mol,K2
③2NO(g)+O2(g)![]() 2NO2(g) △H=-112.3kJ/mol,K3
2NO2(g) △H=-112.3kJ/mol,K3
写出NO与CO反应生成无污染气体的热化学方程式:_____________,此热化学方程式的平衡常数K=_______(用K1、K2、K3表示)
(2)污染性气体NO2与CO在一定条件下的反应为2NO2+4CO![]() 4CO2+N2,某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1个大气压,5秒时反应达到平衡,容器的压强变为原来的
4CO2+N2,某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1个大气压,5秒时反应达到平衡,容器的压强变为原来的![]() ,则反应开始到平衡时CO的平均反应速率v(CO)=_______。若此温度下,某时刻则得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围为________。
,则反应开始到平衡时CO的平均反应速率v(CO)=_______。若此温度下,某时刻则得NO2、CO、CO2、N2的浓度分别为amol/L、0.4mol/L、0.1mol/L、1mol/L,要使反应向逆反应方向进行,a的取值范围为________。
(3)研究发现:NOx是雾霾的主要成分之一,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。已知:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) △H=-1810kJ/mol
①相同条件下,在2L恒容密闭容器中,选用不同的催化剂,上述反应产生N2的物质的量随时间变化的情况如图所示。
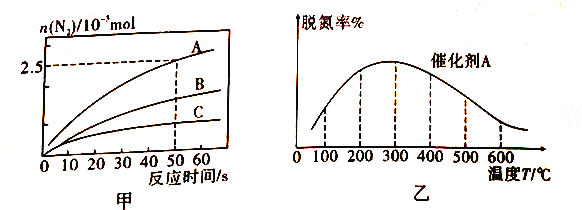
a.在催化剂A作用下,反应达到平衡的标志是_____(填序号)。
A.4v(NH3)正=6v(H2O)逆
B.容器内总压强不再改变
C.容器内密度不再改变
D.NO 和H2O(g)浓度相等
E.容器内平均摩尔质量不再改变
b.在A、B,C 三种催化剂下,清除氮氧化物反应的活化能分别表示为Ea(A)、Ea(B)、Ea(C),根据图甲所示曲线,判断三种催化剂条件下,活化能由大到小的顺序为________。
②在氨气足量时,反应在催化剂A 作用下,经过相同时间,测得脱氮潮殖反应温度的变化情况如图乙所示,据图可知,自相同的时间内,温度对脱氮率的影响及可他的原因是________。(已知A、B催化剂在此温度范围内不失效)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是( )
A.作还原剂
B.作氧化剂
C.既作氧化剂又作还原剂
D.既不作氧化剂又不作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氢吡喃(DHP)常用作有机合成中的保护基。
(1)按照如下路线可以制得DHP。

①单糖A的分子式为_____, DHP分子的核磁共振氢谱有_____组峰。
②1mol糠醛与3mol H2反应转化为B,则B的结构简式为_____。
③ DHP的同分异构体中,属于链状有机物且能发生银镜反应的有_____种。
(2)已知:i. DHP的保护和脱保护机理为
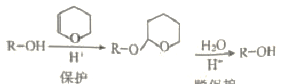
ii. R-C≡CNa + R1OH → R-C≡CH + R1ONa
iii. R-C≡CNa + R1Br → R-C≡C-R1+ NaBr
应用DHP作保护基合成梨小食心虫性外激素的路线如下:
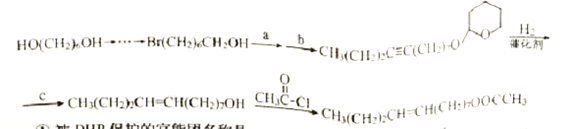
①被DHP保护的官能团名称是_______,保护反应的类型是 ______。
②上述路线中最后一步反应的方程式为 ______。
③上述路线中步骤a、b、c分别为_______、 ______、_______。(例:  )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、选择下列实验方法分离物质,将分离方法的字母填在横线上。
A.萃取分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法 F.升华法
(1)______________分离饱和食盐水与沙子的混合物。
(2)______________分离水和汽油的混合物。
(3)______________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)_____________从碘的水溶液里提取碘。
Ⅱ、蒸馏是实验室制备蒸馏水的常用方法。
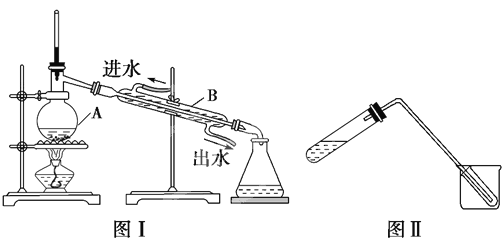
(1)图Ⅰ是实验室制取蒸馏水的常用装置,图中明显的错误是_____________________。
(2)仪器A的名称是______________,仪器B的名称是______________。
(3)实验时A中除加入少量自来水外,还需加入少量________________,其作用是________________________________________。
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ完全相同。该装置中使用的玻璃导管较长,其作用是_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com