


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液体分层,上层为四氯化碳层,黄色 |
| B、液体分层,上层为水层,紫色 |
| C、液体分层,下层为四氯化碳层,紫色 |
| D、液体分层,下层为水层,黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用pH试纸检验气体的酸碱性时,一定要先用蒸馏水润湿 |
| B、润洗滴定管:从滴定管上口加入所要盛装的酸或碱溶液至“0”刻线,再将液体从滴定管下部放出,重复操作2~3次 |
| C、用瓷坩埚加热熔化碳酸钠固体 |
| D、Mg和Al分别为电极,插入NaOH溶液中,构成原电池,探究Mg、Al的活泼性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
| A、①② | B、②④ | C、③④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 非电解质 | 强电解质 | 碱 | |
| A | 漂白粉 | Cl2 | NaCl溶液 | 氨水 |
| B | 盐酸 | NH3 | CH3COOH | Cu2(OH)2CO3 |
| C | 胆矾 | SO2 | Ba(OH)2 | 纯碱 |
| D | Fe(OH)3胶体 | C2H5OH | CaCO3 | 苛性钠 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 若反应为2A(g)+B(g)?2C(g),则△H>0,P2>P1 |
B、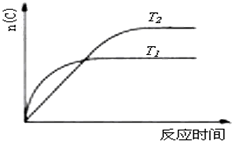 若反应为2A(g)?C(g),则△H>0,T1>T2 |
C、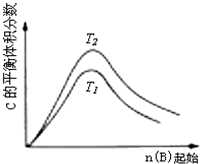 反应为3A(g)+B(g)?2C(g),则△H>0,T2>T1;或△H<0,T2<T1 |
D、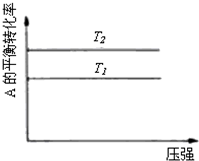 反应为A(g)+B(g)?2C(g),则△H<0,T2>T1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 初始浓度c/mol?L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.001 0 | 290 |
| ② | 1.60 | 0.20 | 0.001 0 | 145 |
| ③ | 0.80 | 0.40 | 0.001 0 | 145 |
| ④ | 0.80 | 0.20 | 0.002 0 | 580 |
| A、增大c(CH3COCH3),v(Br2)增大 |
| B、实验②和③的v(Br2)相等 |
| C、增大c(HCl),v(Br2)增大 |
| D、增大c(Br2),v(Br2)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于0.3 mol |
| B、小于0.3 mol |
| C、大于0.3 mol,小于0.6 mol |
| D、以上结论都不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com