
 ,其一氯代物的结构简式是
,其一氯代物的结构简式是 ;其中一氯代物种类最多的是
;其中一氯代物种类最多的是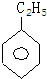 .(均填结构简式)
.(均填结构简式) 分析 分子式为C8H10de烃含苯环的结构,为苯的同系物,为乙苯或二甲苯,二甲苯有邻、间、对三种;苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少,为对二甲苯;含有苯环的同分异构体中,一氯代物种类最多,则分子中H原子种类最多,为乙苯.
解答 解:分子式为C8H10的烃含苯环的结构,为苯的同系物,为乙苯或二甲苯,二甲苯有邻、间、对三种,故4种同分异构体;苯环上的一个氢原子被氯原子取代后产生同分异构体数目最少,为对二甲苯,结构简式为: ,其一氯代物的结构简式为
,其一氯代物的结构简式为 ;
;
含有苯环的同分异构体中,一氯代物种类最多,则分子中H原子种类最多,为乙苯,结构简式为: ;
;
故答案为:4; ;
; ;
; .
.
点评 本题考查有机物分子式确定、同分异构体,难度中等,注意掌握利用相对分子质量确定烃的组成.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| 选项 | R | W | X | Y | Z |  |
| A | Si | SiO2 | H2SiO3 | Na2SiO3 | SiCl4 | |
| B | Na | Na2O | Na2O2 | Na2CO3 | NaOH | |
| C | Fe | Fe(OH)2 | FeCl2 | FeCl3 | Fe(NO3)3 | |
| D | Al | NaAlO2 | Al2(SO4)3 | AlCl3 | Al(NO3)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
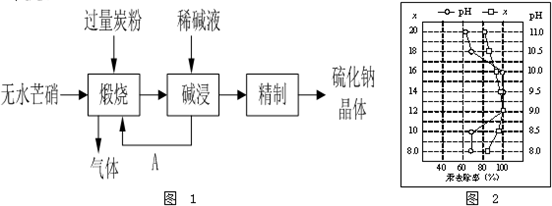
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
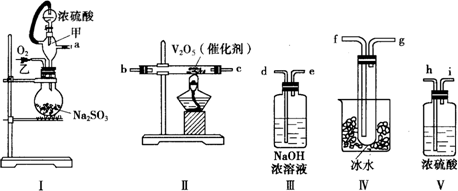
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
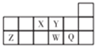
| A. | 离子Y2-和Z3+的核外电子排布相同 | |
| B. | X3-的离子半径小于Z3+的离子半径 | |
| C. | 元素Y的最高正价与最低负价绝对值之和为8 | |
| D. | 元素W的气态氢化物的稳定性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl沉淀生成和沉淀溶解不断进行,但速率相等 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | 在AgCl沉淀溶解平衡体系中加入蒸馏水,AgCl的Ksp增大 | |
| D. | AgCl在相同浓度的CaCl2和NaCl溶液中的溶解度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com