
【题目】现有三组混合物:①CCl4和NaCl的混合液;②苯(沸点:80.1℃)和甲苯(沸点:110.6℃)的混合溶液(苯和甲苯是性质非常相似的一对互溶液体);③掺有碘化钾的碘水,分离以上各混合液的正确方法依次是
A. 分液、蒸馏、萃取 B. 萃取、蒸馏、分液
C. 蒸馏、萃取、分液 D. 分液、萃取、蒸馏
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】已知水的电离平衡曲线如图所示,试回答下列问题:

(1)图中五点kw间的关系是_____________。
(2)若从A点到D点,可采用的措施是 。
a.升温 b.加入少量的盐酸 c.加入少量的NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加压降温可以使空气液化,在此过程中,下列说法正确的是
A.空气中的分子质量变大 B.空气中的分子间隔变小
C.空气中的分子种类改变 D.空气中的分子数目变少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5L 1mol/L FeCl3溶液与0.2L 1mol/L KCl溶液中的Cl﹣的物质的量浓度之比( )
A.5:2
B.3:1
C.15:2
D.1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的温度和压强下,4个相同体积的密闭容器中分 别装有4种气体.则4个容器中气体的质量最大是( )
A.CO2 ,
B.O2
C.N2
D.CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物有广泛的用途。
(1)C(s)+H2O(g)![]() CO(g) +H2(g) ΔH= +131.3 kJ·mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2的产率的是 。(填序号)
CO(g) +H2(g) ΔH= +131.3 kJ·mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2的产率的是 。(填序号)
A.升高温度 B.增加碳的用量
C.加入催化剂 D.用CO吸收剂除去CO
(2)又知,C(s)+ CO2(g)![]() 2CO(g) △H=+172.5kJ·mol-1
2CO(g) △H=+172.5kJ·mol-1
则CO(g)+H2O(g)![]() CO2(g)+H2(g)的△H= 。
CO2(g)+H2(g)的△H= 。
(3)CO与H2在一定条件下可反应生成甲醇,甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
t / min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其他条件不变,降低温度,反应达到新平衡前v(逆)________v(正)(填“>”、“<”、“=”)
②该温度下此反应的平衡常数K=___________
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数___________(填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能用勒沙特列原理解释的是( )
A.Fe(SCN)3溶液中加入固体KSCN后颜色变深
B.棕红色NO2加压后颜色先变深后变浅
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.H2、I2、HI平衡混和气加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在恒温条件下,将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
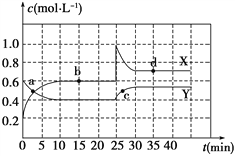
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):____________________。
(2)0~10min化学反应速度V(X)=__________________。
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10)_______ v(10~20)(填“<”、“>”或“=”),原因是________________。
(4) a、b、c、d四个点中,表示化学反应处于平衡状态的点是_________,理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com