
分析 Zn、Pt和电解质溶液构成原电池,Zn作负极、Pt作正极,负极上锌失电子发生氧化反应生成锌离子,正极上氧气得电子发生还原反应生成水,以此解答该题.
解答 解:Zn、Pt和电解质溶液构成原电池,Zn作负极、Pt作正极,电解质溶液呈酸性,正极上氧气得电子发生还原反应生成水,电极反应式为O2+4e-+4H+=2H2O,
负极上锌失电子发生氧化反应生成锌离子,电极反应式为Zn-2e-=Zn2+,
答:负极:2Zn-4e-=2Zn2+正极:O2+4H++4e-=2H2O.
点评 本题考查原电池原理,侧重考查学生书写电极反应式,明确溶液酸碱性是解本题关键,电解质溶液酸碱性不同其电极反应式不同,书写要仔细揣摩.


科目:高中化学 来源: 题型:选择题
| A. | 5min内用B表示的反应速率为0.018mol/(L•min) | |
| B. | 在该温度下反应的平衡常数为900 | |
| C. | A和B的平衡转化率都为90% | |
| D. | 如果加压,平衡正向移动,可使△H 减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
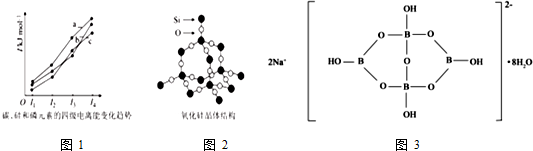
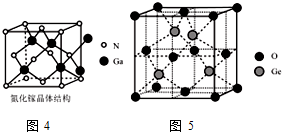
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
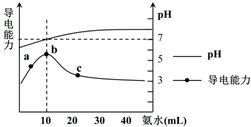
| A. | a~b点导电能力增强说明HR为弱酸 | |
| B. | b点溶液pH=7说明NH4R没有水解 | |
| C. | c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b-c任意点溶液均有c(H+)•c(OH-)=Kw=1.0×10-14 mol2•L-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
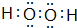 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| C. | 含4.8g碳元素的石墨晶体中的共价键数为1.2NA个 | |
| D. | 2mL 0.5mol/L硅酸钠溶液中滴入过量盐酸制备硅酸胶体,所得胶粒数目为0.001NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
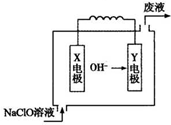
| A. | 镁作Y电极 | |
| B. | 电池工作时Na+向负极移动 | |
| C. | 废液的pH大于NaClO溶液的pH | |
| D. | X电极上发生的反应为:ClO-+2H2O-4e-═ClO3-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②③ | C. | 只有①②③ | D. | 全部正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com