
(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+ 4 NO2 (g)= 4 NO(g)+ CO2 (g)+ 2 H2O(g)ΔH= -574 kJ · mol-1
CH4(g)+ 4 NO(g)= 2 N2(g)+ CO2 (g)+ 2 H2O(g)ΔH= -1160 kJ· mol-1
(1)若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为
(阿伏加德罗常数的值用NA表示),放出的热量为 kJ。
(2)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_______________________________。
(3)甲硅烷(SiH4)是一种无色液体,遇到空气能发生爆炸性自燃,生成(SiO2)和水。已知室
温下10 g甲硅烷自燃放出热量446 kJ,表示其燃烧热的热化学方程式为:
________________________________________________________________________。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1 mol Cl2参与反应时释放145 kJ的热量,写出这个反应的热化学方程式:
_________________________________________________________________________。
(1)1.6NA,173.4
(2)1/2H2SO4(aq) + NaOH(aq) = 1/2Na2SO4(aq) + H2O (l) ΔH=-57.3 kJ·mol-1
(3)SiH4(l)+2O2(g)===SiO2(s)+2H2O(l) ΔH=-1427.2 kJ/mol
(4)2Cl2(g)+2H2O(g)+C(s)===4HCl(g)+CO2(g) ΔH=-290 kJ/mol
【解析】
试题分析:(1)由题中的热力学方程式,可知
2CH4(g)+ 4 NO2 (g)=" 2" N2(g)+ 2CO2 (g)+4 H2O(g)ΔH=-1734 kJ· mol-1,该反应转移的电子数为8,标准状况下4.48L CH4为0.2mol,所以转移的电子总数为1.6NA,放出的热量为173.4kJ;(2)1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,其热化学方程式为1/2H2SO4(aq) + NaOH(aq) = 1/2Na2SO4(aq)
+ H2O (l) ΔH=-57.3 kJ·mol-1;(3)中根据题意先写出化学方程式,SiH4(l)+2O2(g)===SiO2(s)+2H2O(l) ,已知10 g甲硅烷自燃放出热量446 kJ,所以1mol放出的热量为446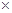
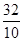 kJ=1427.2 kJ,所以其热化学方程式为
kJ=1427.2 kJ,所以其热化学方程式为
SiH4(l)+2O2(g)===SiO2(s)+2H2O(l) ΔH=-1427.2 kJ/mol,(4)中根据题意先写出化学方程式,2Cl2(g)+2H2O(g)+C(s)===4HCl(g)+CO2(g),放出的热量为145 kJ×2=290kJ,所以其热力学方程式为2Cl2(g)+2H2O(g)+C(s)===4HCl(g)+CO2(g) ΔH=-290 kJ/mol 。
考点:热力学方程式
点评:本题考查了根据给出的现象书写热力学方程式,是高考考查的重点,本题的信息量较大,有一定的难度。


科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)当用酸性电解质时,电极反应式为:负极:__________,正极:__________。
(2)当用碱性电解质时,电极反应式为:负极:__________,正极:__________。
(3)用固体氧化物作电解质时,电极反应式为:负极:__________,正极:__________。
(4)如把H2改CH4 ,KOH作导电物质,则电极反应式为:负极:__________,正极:__________,总反应式:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市丰台区第一次模拟理综化学试卷试卷(解析版) 题型:填空题
(13分)直接排放氮氧化物会形成酸雨、雾霾,催化还原法和氧化吸收法师常用的处理方法。
(1)用化学方程式表示NO2形成酸雨的过程____________________________
(2)利用NH3和CH4等气体除去烟气中的氮氧化物。
①NH3的电子式
②热稳定性 NH3 CH4(填“>”=“<”)
③已知:CH4(g)+2O2(g)=CO2(g)+2H20(l) △H1=akJ/mol; 欲计算反应CH4(g)+4NO(g)=CO2(g)+2H20(l)+2N2(g)的焓变 △H2 则还需要查询某反应的焓变△H3,当反应中各物质的化学计量数之比为最简整数比时,△H3=bkJ/mol,该反应的热化学方程式是__________________________据此计算出△H2= kJ/mol (用含a、b的式子表示)。
(3)利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.写出氧化吸收法除去氮氧化物的化学方程式______________________________________现有标况下的O233.6ml,理论上可以处理该氮氧化物______ml(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:江门一模 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com