

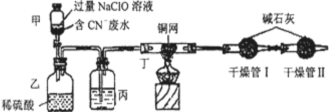
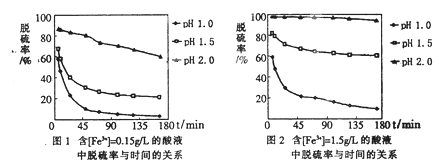


科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验目的 | 操作 |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液 |
| C | 比较盐酸与醋酸的酸性强弱 | 分别测定同温同浓度NaCl与CH3COONa溶液的pH |
| D | 除去苯中混有的苯酚 | 向混合液中加入过量浓溴水,充分反应后,过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
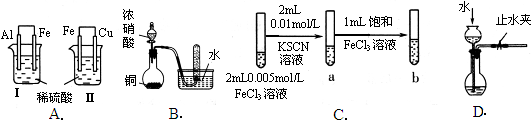
| 实验 | 实验现象 | 结论 |
| A | Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 | 活动性:Al>Fe>Cu |
| B | 试管中收集到无色气体 | 铜与浓硝酸反应产物是NO |
| C | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D | 长颈漏斗内液面高于烧瓶内液面且保持不变 | 装置气密性良好 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
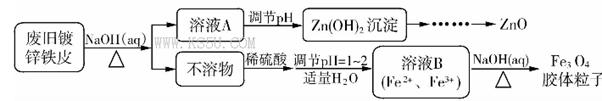
 Fe3O4(胶体)+S4O62-+H2O
Fe3O4(胶体)+S4O62-+H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
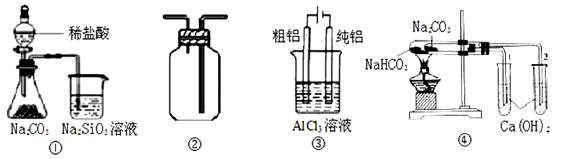
| A.用图①装置验证氯、碳、硅元素非金属性 |
| B.用图②装置能收集O2、CO2和H2 |
| C.用图③装置电解精炼铝 |
| D.用图④装置验证NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

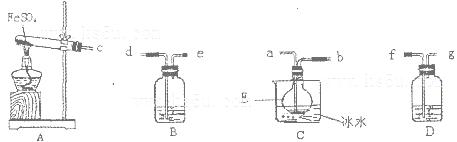
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 (填序号); 试管B中加1%品红溶液; 试管C中加 (填序号)。 | 若___ ___, 则甲成立。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 将CO2(含HC1杂质)通入饱和NaHCO3溶液中 | 除去HC1 |
| B | 向做完银镜反应后的试管中加入稀氨水 | 除去试管内残留物 |
| C | 向做完淀粉水解后的溶液中直接加入新制的Cu(OH)2,并加热 | 检验淀粉是否水解 |
| D | 将少量FeC12试样加水溶解,加稀硝酸酸化,再滴加KSCN溶液 | 检验FeCl2是否变质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
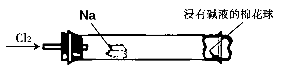
| A.反应生成的大量白色烟雾是氯化钠晶体 |
| B.钠着火燃烧产生苍白色火焰 |
| C.浸有NaOH溶液的棉球用于吸收生成的氯化钠,以免污染空气 |
| D.用湿润的淀粉碘化钾试纸可以检验氯气是否被完全吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com