
| ||
| ||
| ||
| ||
| 9.850g -7.650g |
| 44g/mol |
| ||
| 4.48L |
| 22.4L/mol |
| ||
| m+60 |
| 9.850 |
| m+16 |
| 7.650 |


科目:高中化学 来源: 题型:
| 选项 | 仪器 | 实验目的 |
| A | 分液漏斗 | 分离互不混溶的液体 |
| B | 普通漏斗 | 分离固体与液体 |
| C | 天平 | 称量一定质量的固体 |
| D | 烧杯 | 准确量取一定体积的液体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体粒子直径小于1nm |
| B、胶体粒子不能通过半透膜 |
| C、胶体带电荷,在电场中会定向运动 |
| D、胶体不稳定,静置后容易产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
| B、SiO2既能溶于NaOH溶液又能溶于HF溶液,说明SiO2是两性氧化物 |
| C、乙烯能使溴水、酸性高锰酸钾溶液褪色,说明乙烯具有漂白性 |
| D、铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,因为铁钉表面形成了一层致密稳定的氧化膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13C与14C |
| B、CH3CH2OH与CH3COOH |
| C、甲烷与丙烷 |
D、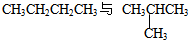 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com