
【题目】在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
a(干燥气体) | b(液体) |
| |
A | NO | 水 | |
B | CO2 | 饱和NaHCO3溶液 | |
C | Cl2 | 饱和NaCl溶液 | |
D | NH3 | 1 mol·L-1盐酸 |
A.AB.BC.CD.D
【答案】D
【解析】
A、一氧化氮和水不反应,所以不能形成喷泉实验,A错误;
B、CO2与饱和NaHCO3溶液不反应,不能形成喷泉实验,B错误;
C、Cl2不溶于饱和氯化钠溶液,也不与其反应,锥形瓶与烧瓶内压强相等,不能形成喷泉,C错误;
D、NH3与盐酸能发生反应,生成物为氯化铵固体,气体被吸收进溶液中,烧瓶内压强减小为零,同外界大气压产生压强差,所以形成喷泉,并充满烧瓶,D正确;
答案选D。
【点晴】
可以通过减小烧瓶内压强形成喷泉:①容器内气体极易溶于水;②容器内气体易与溶液中的某种成分发生化学反应而被吸收。当外部的水或溶液接触容器内气体时,由于气体大量溶解或与溶液中的某种成分发生化学反应而被吸收,从而使容器内气压迅速降低,在外界大气压作用下,外部液体迅速进入容器,通过尖嘴导管喷出,形成喷泉。另外还可以通过增大烧瓶外压强,容器内的液体由于受热挥发(如浓盐酸、浓氨水、酒精等)或由于发生化学反应,容器内产生大量气体。使容器内压强迅速增大,促使容器内液体迅速向外流动,也能形成喷泉。例如喷雾器、人造喷泉等均是利用了此原理。


科目:高中化学 来源: 题型:
【题目】下列解释实验事实的离子方程式正确的是
A. 用醋酸检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑
B. 漂白粉溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3-
C. 酸性KI淀粉溶液久置后变蓝:4I-+O2+4H+=2I2+2H2O
D. Na2S溶液使酚酞试液变红:S2-+2H2O![]() 2OH-+H2S
2OH-+H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛,两个常见的固氮反应的平衡常数的对数值(lgK)与温度的关系如图所示:①N2+3H22NH3 ②N2+O22NO;根据图中的数据判断下列说法正确的是( )

A.反应①和②均为放热反应
B.升高温度,反应①的反应速率减小
C.在1000℃时,反应①和反应②体系中N2的浓度一定相等
D.在标准状况下,利用反应①固氮和利用反应②固氮反应程度相差很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质](1)酒石酸钛配合物广泛应用于药物合成。酒石酸(结构如图所示)中羧基氧原子的轨道杂化类型分别是______________
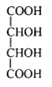
(2)氰酸(HOCN)的结构式是_________,根据等电子体原理,可推测氰酸根离子的空间构型是____。

(3)FeBr2为只含有离子键的离子化合物,其晶胞结构如图a,距一个Fe2+离子最近的所有Br-离子为顶点构成的几何体为_____________.
(4)二茂铁是最重要的金属茂基配合物,也是最早被发现的夹心配合物,包含两个环戊二烯基与铁原子成键.二茂铁的结构为一个铁原子处在两个平行的环戊二烯基环的之间,结构如图b所示,已知二茂铁的一氯代物只有一种.
①二茂铁的分子式为__________.
②穆斯堡尔谱学数据显示,二茂铁中心铁原子的氧化态为+2,每个茂环带有一个单位负电荷.因此每个环含有________个π电子.
③二茂铁中两个茂环可以是重叠的(D5h),也可以是错位的(D5d),它们之间的能垒仅有8~20kJ/mol.温度升高时则绕垂直轴相对转动,使得两种结构可以相互转换,转换过程中能量变化如图c.比较稳定的是__________结构(填“重叠”或“错位”).
(5)氧化镍(NiO)是一种纳米材料,比表面积S(m2/g)是评价纳米材料的重要参数之一(纳米粒子按球形计)。基态Ni2+有_________个未成对电子,已知氧化镍的密度为ρg/cm3;其纳米粒子的直径为Dnm列式表示其比表面积 ____________m2/g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)水能发生自偶电离2H2O![]() H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程式_______。
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程式_______。
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
化学式 | HNO2 | H2N2O2 |
电离常数 | Ka=5.1×10-4 | Ka1=6.17×10-8、Ka2=2.88×10-12 |
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)_____pH(NaHN2O2)(填“>”、“<”或“=”)。
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=_______(保留三位有效数字)。
③0.lmol/LNa2N2O2溶液中离子浓度由大到小的顺序为____________。
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g)![]() NH2CO2NH4(s) △H1=-159.5kJmol-1;
NH2CO2NH4(s) △H1=-159.5kJmol-1;
反应II:NH2CO2NH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1;
反应III:H2O(l)═H2O(g) △H3=+44.0kJmol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为____________。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为___________。
②图2中能正确反应平衡常数K随温度变化关系的曲线为__________(填字母标号)。
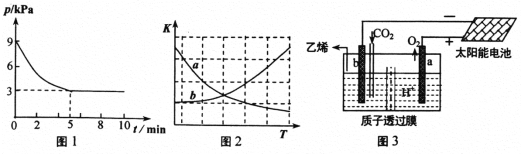
(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )

A.原子半径: Y >Z >X
B.元素气态氢化物的热稳定性:X < Z
C.Y和Z的最高价氧化物对应水化物均为强酸
D.X的最高正价为+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌电池是一种极具前景的电化学储能装置。![]() 扣式可充电电池组成示意图如下。
扣式可充电电池组成示意图如下。![]() 可以在
可以在![]() 晶体中可逆地嵌入和脱除,总反应为
晶体中可逆地嵌入和脱除,总反应为![]() 。下列说法错误的是( )
。下列说法错误的是( )
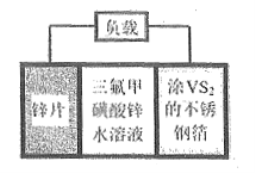
A. 放电时不锈钢箔为正极,发生还原反应
B. 放电时负极的反应为![]()
C. 充电时电池正极上的反应为:![]()
D. 充电时锌片与电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 对2HI(g)![]() H2(g)+I2(g)平衡体系增大压强使气体颜色变深
H2(g)+I2(g)平衡体系增大压强使气体颜色变深
B. 向橙色 K2Cr2O7溶液中加入一定浓度的NaOH溶液后,溶液变为黄色
C. 红棕色的NO2,加压后颜色先变深后变浅
D. 溴水中有下列平衡Br2+H2O![]() HBr +HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr +HBrO,当加入AgNO3溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物中属于芳香烃的是________(填字母),它与苯的关系是________,写出苯与溴发生反应的化学方程式:__________________________。
预测该芳香烃________(填“能”或“不能”)发生该类反应。
![]()
②下列有机物中属于羧酸类的是________(填字母)。
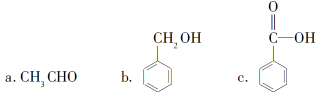
③下列有机物中属于糖类的是________(填字母)。
a.油脂 b.纤维素 c.蛋白质
(2)化合物X的结构简式为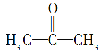 。
。
①一个X分子中有________种等效氢原子。
②X的一种同分异构体Z的结构简式为H2C===CH—CH2OH,请写出Z与Br2发生加成反应的化学方程式: ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com