
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2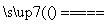 2O3
2O3
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气体的平均摩尔质量为________g/mol(保留一位小数)。
(2)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为________L。
(3)实验 室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热
室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热 后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为________。
后,粉末的质量变为21.6 g。则原混合气中臭氧的体积分数为________。
解析 (1)设原有氧气的物质的量为x mol,已知有30%的氧气转化为臭氧,由反应3O2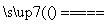 2O3知,发生反应O2的物质的量为0.3x mol,生成O3的物质的量为0.2x mol,故反应后气体的总物质的量为0.9x mol,则得到混合气体的平均摩尔质量为M=
2O3知,发生反应O2的物质的量为0.3x mol,生成O3的物质的量为0.2x mol,故反应后气体的总物质的量为0.9x mol,则得到混合气体的平均摩尔质量为M=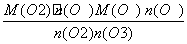
=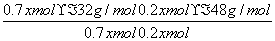
=35.6 g/mol
(2)设反应的O2的体积为a L,则生成O3的体积为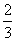 a L,
a L, 由差量法得
由差量法得
3O2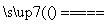 2O3 ΔV
2O3 ΔV
3 2 1
a 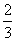 a 1.5 L
a 1.5 L
a=4.5 L,臭氧体积为3 L。
(3)本题应分情况讨论:
①假设O2和O3完全反应,则O2和O3的质量即为铜粉增加的质量,m总=1.6 g,n总=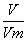 =
=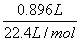 =0.04 mol,则混合气体的平均相对分子质量为
=0.04 mol,则混合气体的平均相对分子质量为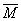 =
=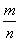 =
=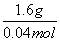 =40 g/mol,
=40 g/mol,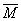 =
=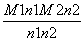 知
知
40 g/mol=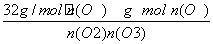
求得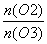 =
=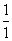
故臭氧体积分数为50%或0.5;
②假设铜完全反应,O2或O3剩余,设生成CuO b g
Cu → CuO
63.5 79.5
20 g b g
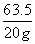 =
=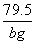 求得b=25>21.6
求得b=25>21.6
故假设错误。
答案 (1)35.6 (2)3 (3)0.5或50%


科目:高中化学 来源: 题型:
已知X为第三周期元素的原子,该原子要达到8 电子稳定结构,则需要的电子数小于其 次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是 ( )
电子稳定结构,则需要的电子数小于其 次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是 ( )
A.X元素最高价氧化物对应的水化物一定是强酸
B.X元素的氢化物的化学式一定为H2X
C.X的单质一定是良好的半导体材料
D.X元素的氧化物一定能与烧碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C 三种醇分别与足量的金属钠反应产生相同体积的氢气,消耗这三种醇的物质的量之比是3:6:2,则A、B、C这三种醇分子种羟基的个数比是:( )
A.3:2:1 B.2:6:3 C.3:6:2 D.2:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下图所示进行反应,又知E溶液是无色的。请回答:
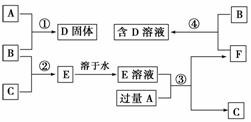
(1)A是________,B是________,C是________。(请填化学式)
(2)反应①的化学方程式为:
_________________ __________________________________________________
__________________________________________________ _____。
_____。
(3)反应③的化学方程式为:
________________________________________________________________________。
(4)反应④的化学方程式为:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )。
A.1.00 mol NaCl中含有6.02×1023个NaCl分子
B.1.00 mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中
D.电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
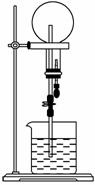
已知NH3和HCl都是能用来做喷泉实验的气体。若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集HCl气体未满,如图所示。喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑溶质的扩散及静止时液面高度的影响) ( )。
A.溶质的物质的量浓度相同 、溶质的质量分数不同
、溶质的质量分数不同
B.溶质的质量分数相同、溶质的物质的量浓度不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列各题所给出的数据,可分别求出其“溶质的质量分数”或“溶质的物质的量浓度”,试判断并求解。
(1)设NA表示阿伏加德罗常数的数值,若某氢氧化钠溶液V L中含有N个OH-,则可求出此溶液中________为________。
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液中________为________。
(3)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中________为________。
(4)已知将100 mL氯化铝的水溶液加热蒸干灼烧,可得到白色固体b g,则可求出原氯化铝溶液中________为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是
A. 只有醛类物质才能发生银镜反应B. 甲醛、乙醛、丙醛都没有同分异构体
C. 将2%的稀氨水逐滴加入2%的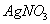 溶液中,至沉淀恰好溶解为止,可制得银氨溶液
溶液中,至沉淀恰好溶解为止,可制得银氨溶液
D. 将2%的NaOH溶液4~6滴,滴入2mL10%的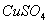 溶液中制得
溶液中制得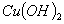 悬浊液,用作检验醛基的试剂
悬浊液,用作检验醛基的试剂
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2O2几乎能与所有常见的气态非金属氧化物在一定条件下反 应,如:
应,如:
2Na2O2+2CO2===2Na2CO3+O2
Na2O2+CO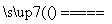 Na2CO3
Na2CO3
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
____________________________________ _____________________________、
_____________________________、
_________________________________________________________________。
(2)通过比较可知,当非金属处于________价态时,与Na2O2反应有O2生成。
(3)等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的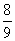 (同温同压下),这时混合气体中N2、O2、CO2物质的量之比为________。
(同温同压下),这时混合气体中N2、O2、CO2物质的量之比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com