
(1)对于下列反应:2SO2 + O2 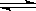 2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
2SO3,如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
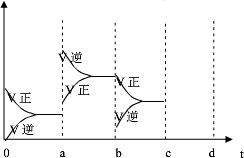
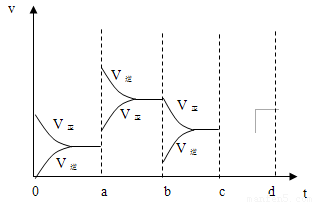
(2)右图表示在密闭容器中反应:2SO2+O2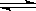 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,
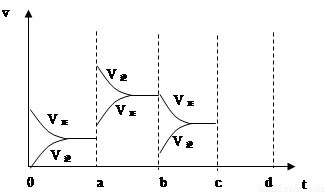
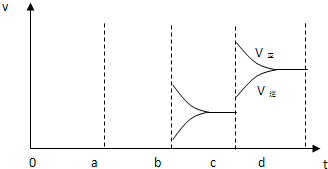
a b过程中改变的条件可能是 ;b c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处.
(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅绿色消失,溶液变成稀盐酸: .
(1)2mol/(L·min); 1mol/(L·min); (2)升温;减小SO3浓度;
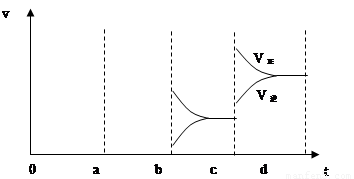
(3)在氯水中存在平衡:Cl2+H2O
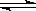 HCl + HClO ,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小.HCl浓度增大,最后浅绿色消失,溶液变成稀盐酸.
HCl + HClO ,HClO见光易分解为HCl和O2,使得平衡体系中HClO浓度减小,平衡向正反应方向移动,Cl2浓度减小.HCl浓度增大,最后浅绿色消失,溶液变成稀盐酸.
【解析】
试题分析:(1)2min内二氧化硫浓度变化为4mol/L,二氧化硫反应速率为2 mol/(L·min),二氧化硫与氧气速率比为2:1。(2) ab过程中反应速率增大且平衡向逆反应方向移动,所以改变的条件是升高温度;bc过程中逆反应速率突然减小、正反应速率逐渐减小,所以改变的条件是改变浓度,平衡向右移动,所以改变的条件是减小生成物浓度;若增大压强,正、逆反应速率均加快,但v(正)>v(逆),平衡向右移动。(3)氯气溶于水的反应是可逆反应,氯水久置,HClO见光分解,次氯酸浓度减少,平衡向右移动,氯气浓度减小,盐酸浓度增大,最终变为稀盐酸。
考点:化学反应速率计算 化学反应速率图像 勒沙特列原理
点评:观察v-t图像时,若增加或减小物质的浓度,则新、旧平衡速率连续;若改变温度、压强、使用催化剂,则正、逆反应速率同时变化,根据v(正)与v(逆)的相对大小判断平衡移动的方向。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)对于下列反应:2SO2+O2?2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为
(1)对于下列反应:2SO2+O2?2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H+(aq) + OH-(aq) = H2O(l) △H =-57.3 kJ·mol-1。
对于下列反应:
①HCl(aq) + NH3·H2O(aq) = NH4Cl(aq) + H2O(l) △H=-a kJ·mol-1
②HNO3(aq) + KOH(aq) = KNO3(aq) + H2O(l) △H =-b kJ·mol-1[
则a、b的大小关系为
A.a>b B.b>a C.a = b D.无法比较
查看答案和解析>>
科目:高中化学 来源:2013届广东省广州市高二上学期期中考试化学(理)试卷 题型:填空题
(1)对于下列反应:2SO2
+ O2 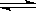 2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
2SO3 , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。
(2)下图表示在密闭容器中反应:2SO2+O2 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
;b c过程中改变的条件可能是
; 若增大压强时,反应速度变化情况画在c~d处.
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是
;b c过程中改变的条件可能是
; 若增大压强时,反应速度变化情况画在c~d处.
(3)请用化学平衡移动知识解释久置的氯水(尤其是长期放置在见光环境),最后浅绿色消失,溶液变成稀盐酸:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com