
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.CaCO3+2HCl═CaCl2+H2O+CO2↑反应中不存在化合价变化,不属于氧化还原反应,故A错误;
B.CaO+H2O═Ca(OH)2反应中不存在化合价变化,不属于氧化还原反应,故B错误;
C.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑反应中Mn、O元素的化合价发生变化,属于氧化还原反应,故C正确;
D.CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑为分解反应,反应中不存在化合价变化,不属于氧化还原反应,故D错误;
E.CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O是CH4的燃烧反应,存在化合价变化,属于氧化还原反应,故E正确;
F.Al(OH)3+3HCl═AlCl3+3H2O反应中不存在化合价变化,不属于氧化还原反应,故F错误;
G.Fe+CuSO4═Cu+FeSO4为置换反应,Cu、Fe元素的化合价发生变化,属于氧化还原反应,故 G 正确;故选:CEG.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
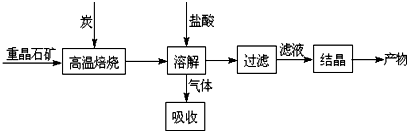
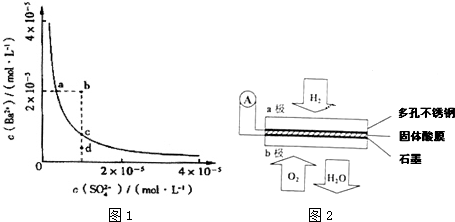
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴离子具有氧化性 | B. | 氯气是还原剂 | ||
| C. | 氯气发生氧化反应 | D. | 氧化性:Cl2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能发生丁达尔效应的分散系是溶液 | |
| B. | 将1 L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| C. | 纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体 | |
| D. | 将饱和FeCl3溶液加热至沸腾,制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.请回答下列问题.
某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| x | 温度 | 压强 | SO2的浓度 | 加入催化剂 |
| y | 容器内气体密度 | CO2的体积分数 | 平衡常数 | CO的转化率 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com