
| �� �� | �� | �� | �� | �� |
| ϡ�������/mL | 100 mL | 200 mL | 300 mL | 400 mL |
| ʣ�����/g | 18.0 g | 9.6 g | 0 | 0 |
| NO���/L | 2.24 L | 4.48 L | 6.72 L | V |
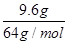 ��2��0.3mol����˵��9.6g��������ͭ��������Һ�к���Fe2�������Լ�������������������NO������V��6.72 L����ѡ��D����ȷ����ѡB��
��2��0.3mol����˵��9.6g��������ͭ��������Һ�к���Fe2�������Լ�������������������NO������V��6.72 L����ѡ��D����ȷ����ѡB��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ�۽�����һԪ�� | B�����۽����Ͷ�Ԫ�� |
| C�����۽����Ͷ�Ԫ�� | D�����۽�����һԪ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1 mol�ǻ��к���10 NA������ |
| B����״���£�2.24 L���к���0.6NA��̼ԭ�� |
| C�����³�ѹ�£�46g NO2��N2O4��������к��е�ԭ������Ϊ3NA |
| D��1 mol Fe��ϡϡ���ᷴӦ����NO���壬ת��2NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1 mol Na2O��Na2O2�Ļ�����к��е�����������������3NA |
| B�������£�1 L 0.1 mol��L-1��NH4NO3��Һ�к��еĵ�ԭ����Ϊ0.2NA |
| C��46 g�л���C2H6O�к��е�H��O������ĿΪNA |
| D����״���£���0.1 mol Cl2ͨ������NaOH��Һ�У���Ӧת�Ƶĵ�����Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1mol 1-��Ȳ�У���2NA���м���9NA���Ҽ� |
| B����O2����ķ�Ӧ�У�1mol O2��������ʱ�õ��ĵ�����һ����4NA |
| C��22��4LHC1����ˮʱ����NA�����ۼ��������� |
| D��17 g����-14CH3������������Ϊ10NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��7.45gNaClO���6.02��1022��NaClO���� |
| B��1.00 molNaClO������ClO���ĵ�������Ϊ26��6.02��1023 |
| C��1 L2 mol/L������ˮ��ɵõ�������������������ĿΪ2��6.02��1023 |
| D����2.00 mol������ȫ����1.00 L ˮ�У��õ���Һ�����ʵ���Ũ��Ϊ2 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1L0.1mol?L�DlNaHCO3��Һ�к���0.1NA��HCO3�D |
| B��17g�����к��е���ԭ����Ϊ3NA |
| C����״���£�2.24LC2H4�к����ۼ���Ϊ0.4NA |
| D�����³�ѹ�£�2.24L�����к��м��������Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1L0.5mol��L��1 ��(NH4)2SO4��Һ�к�NH4+��ΪNA |
| B�����³�ѹ�£�1molCH4�к���4NA��C��H�� |
| C�����³�ѹ�£�48g O3����ԭ����Ϊ2NA�����ԭ��������O 16�� |
| D����״���£�22.4LC6H6(��)�ķ�����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.5 L 1 mol/L NaHS��Һ�У�N(Na+)+N(HS��)=NA |
| B��12.4 g���ף�����ʽΪP4���к���P��P���ۼ�0.6 NA |
| C�������£�pH��2�Ĵ�����Һ�������е�H����Ϊ0.01 NA |
| D����92 g N2O4������������У��ָ������³�ѹʱ���������������ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com