
 (1)已知:O2 (g)═O2+ (g)+e-△H1=+1175.7kJ•mol-1
(1)已知:O2 (g)═O2+ (g)+e-△H1=+1175.7kJ•mol-1分析 (1)利用盖斯定律解答,从待求反应出发,分析待求反应中的反应物和生成物在已知反应中的位置,通过相互加减可得;
(2)①达到化学平衡状态时,正逆反应速率相等,各个组分的浓度不随时间的改变而改变,据此确定是否达到平衡;
②增大压强,化学反应速率加快,根据体积分数结合三行式计算即可;
(3)NH4NO3溶于水,铵根离子水解导致溶液呈酸性,即NH4++H2O?NH3•H2O+H+,c(NH4+)=c(3)铵根离子水解导致溶液显示酸性,根据溶液中的电荷守恒结合溶液显示中性的条件以及电离平衡常数表达式来计算;
(4)甲烷碱性燃料电池中,消耗氢氧化钾,铁棒上镀铜,阴极上的电极反应是:Cu2++2e-=Cu,根据电极反应结合电子守恒来计算.
解答 解:(1)已知:①O2(g)=O2+(g)+e-△H1=+1175.7kJ•mol-1
②PtF6(g)+e-=PtF6-(g)△H2=-771.1kJ•mol-1
③O2+PtF6-(s)=O2+(g)+PtF6-(g)△H3=+482.2kJ•mol-1
反应O2(g)+PtF6(g)=O2+PtF6-(s)可以是①+②-③得到,该反应的焓变△H=(+1175.7kJ•mol-1)+(-771.1kJ•mol-1)-482.2kJ•mol-1=-77.6kJ•mol-1,
故答案为:O2(g)+PtF6(g)=O2+PtF6-(s)△H=-77.6kJ•mol-1;
(2)①a.氮气氢气合成氨气的反应是反应前后系数和减小的反应,体系的压强保持不变,证明达到了平衡状态,故a正确;
b、混合气体的质量在前后是守恒的,体积不变,密度始终保持不变,所以密度不变化学反应不一定平衡,故b错误;
c、N2和H2的体积比为1:3,化学反应不一定平衡,故c错误;
d.混合气体质量前后是守恒的,物质的量变化,所以混合气体的平均摩尔质量会变化,当M不变,证明达到了平衡,故d正确.
故选:a d;
②增大压强,化学反应速率加快,根据图示内容知道,B的压强较大,所以vA(NH3)<vB(NH3),合成氨的反应是放热的,所以温度升高,速率加快,反应的平衡常数减小,因为A点温度低,所以kA>kB,在250℃、1.0×104kPa下达到平衡,氨气的体积分数是50%,则设N2的转化量为x,
N2+3H2?2NH3,
初始量:1 3 0
变化量:x 3x 2x
平衡量:1-x 3-3x 2x
$\frac{2x}{1-x+3-3x+2x}$=50%,解得x=$\frac{2}{3}$,所以氢气的转化率为:$\frac{3×\frac{2}{3}}{3}$×100%=66.7%,故答案为:<;>;66.7.
(3)NH4NO3溶于水,铵根离子水解导致溶液呈酸性,即NH4++H2O?NH3•H2O+H+,c(NH4+)=c(NO3-)=$\frac{a}{b}$mol/L,氨水的Kb=$\frac{c(N{{H}_{4}}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$=2.0×10-5,
当溶液显示中性时,c(OH-)=10-7mol/L,所以$\frac{a}{200b}$mol/L,故答案为:$\frac{a}{200b}$;
(4)甲烷燃料电池中,消耗氢氧化钾,所以pH变小,装置Ⅱ中实现铁棒上镀铜,阴极上的电极反应是:Cu2++2e-=Cu,质量变化了25.6g即生成铜0.4mol,则电子转移了0.8mol,装置Ⅰ燃料做负极,负极a极反应为:CH4-8e-+10OH-=CO32-+7H2O,转移0.8mol电子,会消耗甲烷0.1mol,即2.24L,
故答案为:变小;CH4-8e-+10OH-=CO32-+7H2O;2.24.
点评 本题涉及电化学、热化学、化学反应速率和平衡的影响因素等知识,注意知识的归纳和整理是关键,综合性强,难度大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下22.4L Cl2与足量NaOH溶液反应生成NaCl和NaClO,转移电子数为Na | |
| B. | 16g甲烷中含有的非极性共价键键数为4Na | |
| C. | 一定两点额SO2溶于水后形成pH为2的水溶液,其中H+的数目为0.01Na | |
| D. | 1.8gD2O中含有的质子数为2Na |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ------ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量NaOH固体,c(CH3COO-)减小 | |
| B. | 加入少量FeCl3固体,c(CH3COO-)减小 | |
| C. | 稀释溶液,溶液的pH增大 | |
| D. | 加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 完成下列各题:
完成下列各题:| 容器 | 反应速率 | 容器 | 反应速率 |
| 甲 | v(X)=3.5mol•L-1•min-1 | 乙 | v(Y)=2 mol•L-1•min-1 |
| 丙 | v(Z)=4.5mol•L-1•min-1 | 丁 | v(X)=0.075mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | K1闭合,铁棒上发生的反应为2H++2e-→H2↑ | |
| B. | K1闭合,石墨棒周围溶液pH逐渐降低 | |
| C. | K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法 | |
| D. | K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
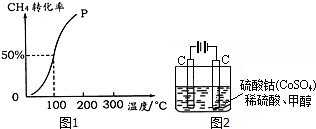
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com