

 ,
,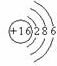 ;
; →
→ ,故答案为:3H?+
,故答案为:3H?+ →
→ .
.


科目:高中化学 来源: 题型:
| A、1molH2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、3.01×1023个SO2分子物质的量为0.5mol |
| D、标准状况下,1mol任何物质体积均为22.4L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 50mL0.2mol?L-1AlCl3溶液中加入2mol?L-1NaOH溶液a mL后,再滴加1 mol?L-1盐酸.滴加盐酸的体积(横坐标)与生成沉淀的质量(纵坐标)的关系如图所示,则加NaOH溶液的体积为( )
50mL0.2mol?L-1AlCl3溶液中加入2mol?L-1NaOH溶液a mL后,再滴加1 mol?L-1盐酸.滴加盐酸的体积(横坐标)与生成沉淀的质量(纵坐标)的关系如图所示,则加NaOH溶液的体积为( )| A、10mL | B、25mL |
| C、50mL | D、60mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com