
【题目】甲醇是一种重要的可再生资源。
(1)已知:2CH4(g)+O2(g) =2CO(g)+4H2(g) △H=akJmol-1
CO(g) +2H2(g)=CH3OH(g) △H=bkJmol-1
写出由CH4和O2制取CH3OH(g)的热化学方程式:____________________________。
(2)反应:CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。
CH3OH(g)的平衡常数K的表达式为________________;甲图是反应时CO和CH3OH(g)的物质的量浓度随时间(t)的变化曲线。从反应开始至达到平衡时,用H2表示的反应速率υ(H2)=________________。
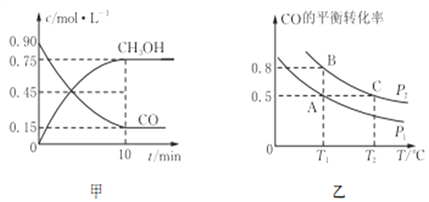
(3)在一容积可变的密闭容器中充入10 mol CO和20 mol H2,发生反应并达到平衡,CO的平衡转化率随温度(T)、压强(P)的变化曲线如图乙所示。
①能判断该反应达到化学平衡状态的是_______(填选项字母)。
A.H2的消耗速率等于CH3OH的生成速率的2倍
B.H2的体积分数不再改变
C.H2的转化率和CO的转化率相等
D.混合气体的平均相对分子质量不再改变
②比较A、B两点压强大小P(A)________P(B)(填“>、<、=”)。
③比较KA、KB、KC的大小:________________。
(4)以甲醇为燃料,O2为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。若KOH溶液足量,写出燃料电池负极的电极反应式:________________________。
【答案】 2CH4(g)+O2(g)=2CH3OH(g) ΔH=(a+2b)kJ·mol-1 K=![]() 0.15mol·L-1·min-1 BD < KA=KB>KC CH3OH-6e-+8OH-=CO32-+6H2O
0.15mol·L-1·min-1 BD < KA=KB>KC CH3OH-6e-+8OH-=CO32-+6H2O
【解析】(1)本题考查热化学反应方程式的计算,甲烷和氧气反应制取甲醇的反应方程式为2CH4+O2→2CH3OH,①2CH4(g)+O2(g) =2CO(g)+4H2(g) ,②CO(g) +2H2(g)=CH3OH(g),①+2×②得出2CH4(g)+O2(g)=2CH3OH(g) △H=(a+2b)kJ·mol-1;(2)本题考查化学平衡常数以及反应速率的计算,根据化学平衡常数的定义,此反应的化学平衡常数的表达式为K=![]() ;根据化学反应速率定义,v(CH3OH)=0.75/10mol/(L·min)=0.075 mol/(L·min),根据化学反应速率之比等于化学计量数之比,即v(H2)=2v(CH3OH)=2×0.075mol/(L·min)=0.15mol/(L·min);(3)本题考查化学平衡状态的判断以及影响化学平衡的因素、影响化学平衡常数的因素,①A、用不同物质的化学反应速率判断达到化学平衡,要求反应方向是一正一逆,且化学反应速率之比等于化学计量数之比,消耗氢气和生成甲醇反应都是向正反应方向移动,因此不能判断是否达到平衡,故错误;B、根据化学平衡常数的定义,当组分的浓度不再改变,说明反应达到平衡,故正确;C、因为投入的物质的量之比与化学计量数之比相等,任何时刻,两者的转化率相等,因此不能判断是否达到化学平衡,故错误;D、根据M=m/n,组分都是气体,气体总质量不变,反应前后气体系数之和不相等,因此平均摩尔质量不变,说明反应达到平衡,故正确;②根据影响化学平衡移动的因素,增大压强,平衡向正反应方向移动,即压强越大,CO的转化率越大,P(A)<P(B);③化学平衡常数只受温度的影响,温度不变,化学平衡常数不变,即KA=KB,随着温度的升高,CO的转化率降低,说明平衡向逆反应方向移动,即正反应方向是放热反应,因此有KC<KA,综上所述KA=KB>KC;(4)通甲醇的一极为负极,通氧气的一极为正极,电解质为KOH,因此负极反应式为CH3OH+8OH--6e-=CO32-+6H2O。
;根据化学反应速率定义,v(CH3OH)=0.75/10mol/(L·min)=0.075 mol/(L·min),根据化学反应速率之比等于化学计量数之比,即v(H2)=2v(CH3OH)=2×0.075mol/(L·min)=0.15mol/(L·min);(3)本题考查化学平衡状态的判断以及影响化学平衡的因素、影响化学平衡常数的因素,①A、用不同物质的化学反应速率判断达到化学平衡,要求反应方向是一正一逆,且化学反应速率之比等于化学计量数之比,消耗氢气和生成甲醇反应都是向正反应方向移动,因此不能判断是否达到平衡,故错误;B、根据化学平衡常数的定义,当组分的浓度不再改变,说明反应达到平衡,故正确;C、因为投入的物质的量之比与化学计量数之比相等,任何时刻,两者的转化率相等,因此不能判断是否达到化学平衡,故错误;D、根据M=m/n,组分都是气体,气体总质量不变,反应前后气体系数之和不相等,因此平均摩尔质量不变,说明反应达到平衡,故正确;②根据影响化学平衡移动的因素,增大压强,平衡向正反应方向移动,即压强越大,CO的转化率越大,P(A)<P(B);③化学平衡常数只受温度的影响,温度不变,化学平衡常数不变,即KA=KB,随着温度的升高,CO的转化率降低,说明平衡向逆反应方向移动,即正反应方向是放热反应,因此有KC<KA,综上所述KA=KB>KC;(4)通甲醇的一极为负极,通氧气的一极为正极,电解质为KOH,因此负极反应式为CH3OH+8OH--6e-=CO32-+6H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙两位同学,他们一起做了如图所示的水果电池实验,测得数据如下表:
实验次数 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
1 | 锌 | 铜 | 菠萝 | 3 | 900 |
2 | 锌 | 铜 | 苹果 | 3 | 650 |
3 | 锌 | 铜 | 柑橘 | 3 | 850 |
4 | 锌 | 铜 | 西红柿 | 3 | 750 |
5 | 锌 | 铝 | 菠萝 | 3 | 650 |
6 | 锌 | 铝 | 苹果 | 3 | 450 |
甲同学提出的问题,乙同学解释不正确的是
①甲:实验6中的负极反应如何写? 乙:铝为负极:Al-3e-===Al3+
②甲:实验1、5电流方向为什么相反? 乙:实验1中锌为负极,电流由铜经导线流向锌;实验5中铝为负极,铝失去电子,电流由锌经导线流向铝
③甲:水果电池的电压与哪些因素有关? 乙:只跟水果的品种有关。
A. ③ B. ① C. ①②③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol·L-1的某一元酸(HA)溶液中![]() =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.该一元酸溶液的pH=1
B.该溶液中水电离出的c(H+)=1×10-11molL-1
C.该溶液中水的离子积常数为1×1022
D.用 pH=11的NaOH 溶液 V1 L 与V2 L 0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在透明溶液中,不能大量共存的离子组是( )AC
A.Cu2+、Na+、SO42-、Cl- B.K+、Na+、HCO3-、NO3-
C.OH-、HCO3-、Ca2+、Na+ D.Ba2+、Na+、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
电离平衡常数(25 ℃) | Ka=1.77 ×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)在温度相同时,各弱酸的Ka值与酸性的相对强弱的关系为________________。
(2)室温下①0.1 mol·L-1 HCOONa,②0.1 mol·L-1 NaClO,③0.1 mol·L-1 Na2CO3,④0.1 mol·L-1 NaHCO3溶液的pH由大到小的关系为______________________。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO![]() 、CO
、CO![]() 、HSO
、HSO![]() 、HCO
、HCO![]() 浓度从大到小的顺序为____________________________。
浓度从大到小的顺序为____________________________。
(4)下列离子方程式正确的是________(填字母)。
a.2ClO-+H2O+CO2=2HClO+CO![]()
b.2HCOOH+CO![]() =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO![]()
d.Cl2+H2O+2CO![]() =2HCO
=2HCO![]() +Cl-+ClO-
+Cl-+ClO-
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是( )
A. 950mL,111.2g B. 950mL,117.0g
C. 1000mL,117.0g D. 1000mL,111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧的含量是衡量水质的一个重要指标,某实验兴趣小组通过如下步骤来测量水中溶解氧的含量:
步骤一:向溶解氧测量瓶中注入20.00 mL水样,再分别加入1 mL 0.1 mol L-1MnSO4溶液和3mL NaOH和KI的混合溶液,充分反应。此时发生反应的化学方程式为: Mn2++2OH-=Mn(OH)2↓ 2Mn(OH)2+ O2 =2MnO(OH)2
步骤二:向上述混合物中加入1.5 mL浓硫酸,充分反应后制沉淀完全溶解,此时溶液呈黄色。
步骤三:将溶液全部转移到容量瓶中,向其中滴加23滴淀粉溶液,溶液呈蓝色。用 0.005 mol L-1的Na2S2O3标准溶液滴定至蓝色恰好消失,共消耗Na2S2O3标准溶液3.60 mL。此时发生反应为:
I2+2Na2S2O3= 2NaI + Na2S4O6
(1)25 ℃时,步骤一中当加入NaOH使溶液的pH = 12时,此时溶液中的c(Mn2+)=_________mol L-1 。 (已知 KspMn(OH)2 =2.06×10-13)
(2)写出步骤二中所发生反应的化学方程式:______________________________。
(3)计算该水样中溶解氧的含量。(单位:mg L-1,请写出计算过程)______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。
N2(g)+2CO2(g)各容器中起始物质的量浓度与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随间变化关系如下图所示。
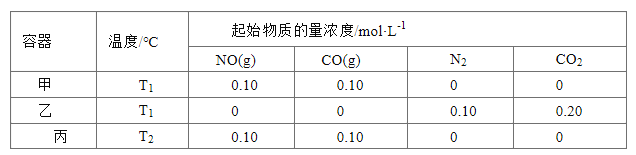
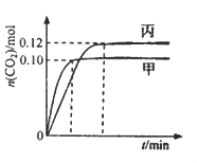
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 乙容器中反应达到平衡时,N2的转化率小于50%
C. 达到平衡时,乙容器中的压强一定大于甲容器的2倍
D. 丙容器中反应达到平衡后,再充入0.10mol NO和0.10mol CO2,此时v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某一元弱酸(HA)和氢氧化钠溶液混合后溶液呈中性,则此溶液中c(Na+)与c(A-)的关系为( )
A. c(Na+)=c(A-) B. c(Na+)<c(A-) C. c(Na+)>c(A-) D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com