
| A. | 剩余固体是铁、铜混合物 | B. | 原固体混合物中铜的质量是12.4g | ||
| C. | 反应后溶液中n(Fe3+)=0.10mol | D. | 反应后溶液中n(Fe2+)+N(Cu2+)=1mol |
分析 铁比铜活泼,与FeCl3溶液反应时先后发生Fe+2Fe3+=3Fe2+、Cu+2Fe3+=Cu2++2Fe2+,原氯化铁溶液中含有氯化铁的物质的量为n(FeCl3)=5mol/L×0.1L=0.5mol,结合反应的方程式解答.
解答 解:A.铁的还原性强于铜,把铁、铜混合粉末加入氯化铁溶液中,铁先与铁离子反应,氯化铁的物质的量是0.5mol,
设0.5mol铁离子完全反应消耗铁、铜的质量分别为m1、m2,则:
Cu+2Fe3+=Cu2++2Fe2+ Fe+2Fe3+=3Fe2+
64g 2mol 56g 2mol
m1 0.5mol m2 0.5mol
解得:m1=16g,m2=14g,
溶解的金属质量为:18g-2.8g=15.2g,14g<15.2g<16g,则铁完全反应、铜部分反应,且Fe3+完全反应,剩余的金属为Cu,故A、C错误;
B.设反应消耗铜的物质的量为n1,反应的铁的物质的量为n2,
则:①64n1+56n2=15.2g ②n1+n2=$\frac{1}{2}$n(Fe3+)=0.25mol,解得:n1=0.15mol、n2=0.1mol,
则原来混合物中含有的铜的质量为:0.15mol×64g/mol+2.8g=12.4g,故B正确;
C.Fe3+完全反应,剩余的金属为Cu,故C错误;
D.根据反应方程式可知反应后溶液中n(Fe2+)=2n(Cu)+3n(Fe)=2×0.15mol+3×0.10mol=0.6mol,
反应后溶液中铜离子的物质的量为n(Cu2+)=n(Cu)=0.15mol,故n(Fe2+)+n(Cu2+)=0.6mol+0.15mol=0.75mol,故D错误.
故选B.
点评 本题考查混合物的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意根据反应的相关方程式从质量守恒的角度解答,题目难度中等.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料表 | 精制海盐、碘酸钾(KIO3) |
| 含碘盐 | 20~40mg/kg |
| 储藏方法 | 密封避光、防潮 |
| 使用方法 | 烹调时待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量CO2通入Ca(ClO)2溶液中:CO2+H2O+Ca2++2ClO-═CaCO3↓+2HClO | |
| B. | 氢氧化铜加到醋酸溶液中:Cu(OH)2+2H+═Cu2++2H2O | |
| C. | 向FeCl3溶液中加入铜粉:2Fe3++Cu═Cu2++2Fe2+ | |
| D. | 过量的氨水滴加到氯化铝溶液:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol•L-1的NaOH溶液:K+、Ba2+、Cl-、NO3- | |
| B. | 0.1mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1mol•L-1的FeCl3溶液:K+、NH4+、NO3-、Cl- | |
| D. | 0.1mol•L-1的HCl溶液:K+、Na2+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ④⑤ | C. | ③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
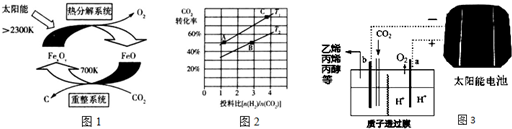
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
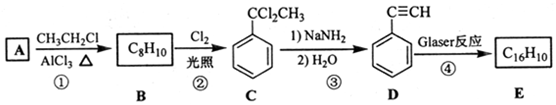
 ,D 的化学名称为苯乙炔.
,D 的化学名称为苯乙炔. .用1mol E合成1,4-二苯基丁烷,理论上需要消耗氢气4mol.
.用1mol E合成1,4-二苯基丁烷,理论上需要消耗氢气4mol.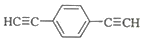 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为n
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为n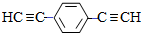 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$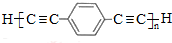 +(n-1)H2.
+(n-1)H2.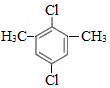 ,
, .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com