
【题目】与铁相似,金属锡能与盐酸反应生成氯化亚锡(SnCl2),氯化亚锡又能被氯化铁氧化为氯化锡(SnCl4)。则下列有关粒子氧化性和还原性强弱的比较中,正确的是
A.氧化性:Sn4+<Sn2+B.氧化性:Fe3+<Sn4+
C.还原性:Fe2+<Sn2+D.还原性:Fe<Sn
科目:高中化学 来源: 题型:
【题目】下列化学工艺流程不可行的是
A. 实验室从海带中提取单质碘:取样→灼烧→溶解→过滤→萃取→蒸馏
B. 石英砂![]() 粗硅
粗硅![]() 粗SiCl4
粗SiCl4![]() 高纯硅
高纯硅
C. FeS2![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx、SO2是常用的化工原料,含NOx、SO2的烟气大量排放能造成严重的大气污染。
(1)含NH3、NOx、SO2的烟气在大气中相互作用,产生的雾霾颗粒中有多种无机盐,其中无机铵盐主要是_____________(填化学式,只写两种)。
(2)SO2催化氧化反应2SO2(g)+O2(g)![]() 2SO3(g)的能量与反应进程如图所示:
2SO3(g)的能量与反应进程如图所示:
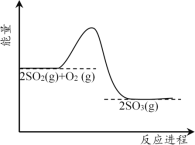
①该反应的正反应为____热(填“放”或“吸”)反应。
②若该反应在恒温恒容密闭容器中进行,能说明该 反应已达到化学平衡状态的是____(填标号)。
A.SO2的v(正)=v(逆)
B.混合气体中同时存在SO2、O2、SO3
C.容器内混合气体密度不随时间而变化
D.容器内混合气体总压强不再随时间而变化
(3)Wang c H等研究发现用Fe2O3/CeO2作催化剂,可用乙烯脱除烟气中SO2并回收单质硫。反应原理为:CH2=CH2+3SO2![]() 3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
3S+2CO2+2H2O。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
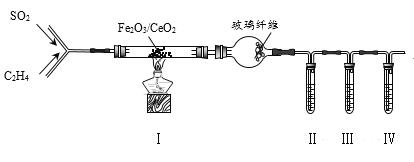
①实验中所需SO2可由Cu与浓硫酸反应制取,该反应的化学方程式为________。
②已知:酸性KMnO4可将CH2=CH2氧化为CO2;装置Ⅱ、Ⅲ中试剂均足量;装置(Ⅰ)的尾气中还含有未反应的SO2和CH2=CH2。检验CO2时,Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次可以是_____(填标号)。
A.酸性KMnO4溶液、品红溶液、澄清石灰水
B.NaOH溶液、酸性KMnO4溶液、澄清石灰水
C.Br2的H2O溶液、品红溶液、澄清石灰水
D.Br2的CCl4溶液、酸性KMnO4溶液、澄清石灰水
(4)取用氨水脱除烟气中SO2得到的副产品[只含(NH4)2SO4和NH4HSO4] 3.875g,与足量NaOH混合后加热充分反应,共收集到氨气1.232L(已折合为标准状况),则该副产品中(NH4)2SO4和NH4HSO4的物质的量之比n[(NH4)2SO4]∶n(NH4HSO4)=______(写出计算结果即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于C60、H3、O2-、N5+等微粒的叙述错误的是
A. 碳、氢、氧、氮元素各含有不同核素
B. H3与H2化学性质相同,互为同位素
C. C60与N5+中都含有共价键
D. KO2属于含有共价键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)常作火箭发射的推进剂,在400℃时开始分解,产物为N2、Cl2、O2、H2O,用以下装置进行NH4ClO4分解实验。下列有关叙述正确的是
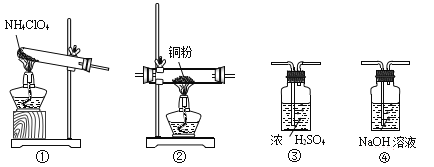
A. 高氯酸铵分解产生的Cl2、N2、O2都可用排空气法收集
B. 可按①③②④的连接顺序制得干燥纯净的N2
C. 1mol NH4ClO4分解,标准状况下收集到气体体积为44.8L
D. 装置①也可用于实验室加热NH4Cl或NH4NO3制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,b、d是运用有机合成制备的具有立体结构的有机物,p、m是广泛存在于动植物体内萜类化合物,下列说法正确的是
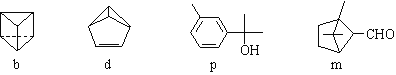
A. b与d互为同分异构体,p与m互为同分异构体
B. b、d、p中,只有p的所有碳原子在同一个平面上
C. d、p、m均可与酸性高锰酸钾溶液反应
D. b的二氯代物有三种,d与H2加成后的产物的一氯代物有四种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图表示反应N2(g)+3H2(g)![]() 2NH3(g); ΔH=-92.2kJ/mol。 在某段时间t0~ t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是 ( )
2NH3(g); ΔH=-92.2kJ/mol。 在某段时间t0~ t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是 ( )
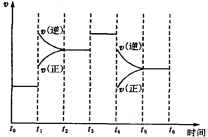
A、t0—t1 B t2—t3 C t3—t4 D t5—t6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋具有十分巨大的开发潜力,人们可以从海水中获得多种物质.工业上进行海水淡化有多种方法.
(1)蒸馏法是历史悠久,技术和工艺比较成熟的海水淡化方法,如图1是海水蒸馏法装置示意图,仪器B的名称是__________。
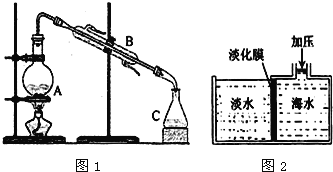
(2)图2是膜分离技术进行淡化的原理示意图,水分子可以透过淡化膜,而海水中其他各种粒子不能通过淡化膜,加压后,右侧海水中减少的是______(填字母)。
A.溶质质量 B.溶剂质量 C.溶质的物质的量浓度
Ⅱ.从海水中提取一些重要的化工产品的工艺流程如图所示。
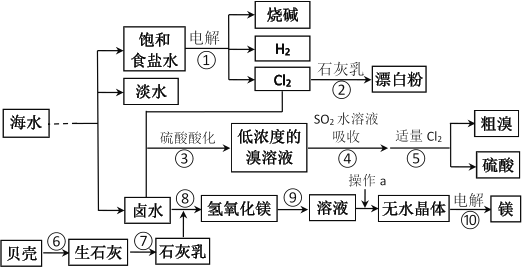
根据上述流程图回答下列问题:
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是________NA。
(4)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是_______________。
(5)过程⑥⑦⑧⑨⑩中没有涉及的化学反应类型是______。
A.分解反应 B.化合反应 C.复分解反应 D.置换反应
(6)写出反应④与⑩的化学方程式
④________________________________________________;
⑩________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于溶液的下列说法不正确的是( )
A. 某温度下,Ba(OH)2溶液中Kw=10-12,向pH=8的该溶液中加入等体积pH=4的盐酸,充分反应后,混合溶液的pH=6
B. 水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-可能大量存在
C. 往0.1mol/LNH4Cl溶液中不断加入NaOH固体,随着NaOH的加入,![]() 不断减小
不断减小
D. 一定温度下,氢氧化钙达到溶解平衡,向此溶液中加入少量氧化钙粉末(不考虑热效应),则溶液中c(Ca2+)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com