
分析 平衡时混合气体总质量等于起始时二氧化硫与氧气总质量,根据n=$\frac{m}{M}$计算平衡时混合气体总物质的量,恒温恒容条件下,压强之比等于物质的量之比;
设参加反应的SO2为xmol,利用三段式表示出平衡时各组分的物质的量,再根据平衡时混合气体总物质的量列方程计算x的值,进而计算平衡体系中SO2的体积分数.
解答 解:平衡时混合气体总质量等于起始时二氧化硫与氧气总质量,即混合气体总质量=3mol×64g/mol+1mol×32g/mol=224g,则平衡时混合气体总物质的量=$\frac{224g}{70g/mol}$=3.2mol,恒温恒容条件下,压强之比等于物质的量之比,故则平衡时体系内压强为P×$\frac{3.2mol}{3mol+1mol}$=0.8P;
设参加反应的SO2为xmol,则:
2SO2(g)+O2(g)?2SO3(g)
开始(mol):3 1 0
转化(mol):x 0.5x x
平衡(mol):3-x 1-0.5x x
所有3-x+1-0.5x+x=3.2
解得x=1.6
故平衡体系中SO2的体积分数为$\frac{1.6mol}{3.2mol}$×100%=50%,
故答案为:0.8P;50%.
点评 本题考查化学平衡的有关计算,难度不大,注意化学平衡计算中三段式的应用.


科目:高中化学 来源: 题型:解答题


 的名称2,3,5-三甲基-4-乙基庚烷
的名称2,3,5-三甲基-4-乙基庚烷 ②氢氧根离子
②氢氧根离子
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .则:
.则: .
.| A→H | A→B | B→C | F→G | |
| 反应类型 |

 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$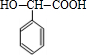 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 3:1 | C. | 3:2 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol•L-1 | B. | 1.0 mol•L-1 | C. | 1.5 mol•L-1 | D. | 2.0 mol•L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-═H2O 2KOH+H2SO4═K2SO4+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com