
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-5mol/L | |
| B. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| D. | 10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |
分析 A、NaB溶液呈碱性,说明NaB为强碱弱酸盐,溶液中存在电荷守恒,根据电荷守恒判断;
B、根据物料守恒分析解答;
C、根据pH相等的三种溶液中,铵根离子水解程度越大,溶液的浓度越大分析;
D、如果HA是强酸,二者浓度相等,要使混合溶液呈中性,则两种溶液体积相等;如果HA是弱酸,则HA浓度大于NaOH,要使混合溶液呈中性,则碱体积大于酸.
解答 解:A、NaB溶液呈碱性,说明NaB为强碱弱酸盐,溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(B-),所以c(Na+)-c(B-)=c(OH-)-c(H+)=10-6mol/L-10-8mol/L=0.99×10-6mol/L,故A错误;
B、根据物料守恒,可知c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C、pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,NH4HSO4电离出H+,NH4+浓度最小,NH4Cl和(NH4)2SO4水解程度相同,正确顺序为①=②>③,故C正确;
D、如果HA是强酸,二者浓度相等,要使混合溶液呈中性,则两种溶液体积相等;如果HA是弱酸,则HA浓度大于NaOH,要使混合溶液呈中性,则碱体积大于酸,所以所得溶液体积(假设混合后的体积是两溶液体积之和)V(总)≤20mL,故D错误;
故选C.
点评 本题考查离子浓度大小比较及酸碱混合溶液定性判断,为考试热点,根据溶液中溶质及其性质再结合守恒思想分析解答,注意D选项要考虑HA的强弱,为易错点.


科目:高中化学 来源: 题型:实验题
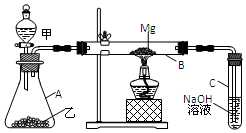 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应:2NO2(红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态).下列说法不正确的是( )
已知反应:2NO2(红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小,且整个操作过程物质均为气态).下列说法不正确的是( )| A. | b点到c点的实验现象是气体颜色先变深后变浅,最后气体颜色比a点还要深 | |
| B. | c点与a点相比,n(NO2)减小,混合气体密度增大 | |
| C. | d 点:v(正)<v(逆) | |
| D. | 若在注射器中对反应H2(g)+I2(g)?2HI(g)进行完全相同的操作,最后能得到相似的透光率变化趋势图象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体中含有的少量杂质SO2可通过饱和Na2CO3溶液除去 | |
| B. | NaOH溶液中含有少量的Ba(OH)2可加入适量的Na2SO4过滤除去 | |
| C. | K2CO3固体中含有少量的NaHCO3杂质可用加热的方式提纯 | |
| D. | Cu粉中含有的少量杂质Fe可加入FeCl3溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用饱和碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| B. | 苯与甲苯互为同系物,均能使酸性KMnO4溶液褪色 | |
| C. | 淀粉和纤维素不是同分异构体,但它们水解的最终产物是同分异构体 | |
| D. | 甲烷和氯气按体积比1:2的比例混合后光照,生成的有机物全部是CH2Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子方程式 | 评价 |
| A | 将2molCl2通入到含lmolFeI2的溶液中:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | 正确:Cl2过量,可将Fe2+、I-均氧化 |
| B | 稀硝酸中加过量铁粉:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | 正确:过量的Fe还原了Fe3+ |
| C | 过量SO2通入到NaClO 溶液中:ClO-+SO2+H2O═HSO3-+HClO | 正确:说明酸性:H2SO3强于HClO |
| D | Mg(HCO3)2溶液与足量的NaOH 溶液反应:Mg2++HCO3-+OH-═MgCO3↓+H2O+CO32- | 正确:酸式盐与碱反应生成正盐和水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 金属钠存放于煤油中 | |
| C. | 浓硝酸保存在棕色试剂瓶中 | |
| D. | 漂白粉长期敞口放置在烧杯中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cu与足量稀硝酸反应产生NA个NO分子 | |
| B. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol•L-1 | |
| C. | 通常条件下,7.1g 37Cl2含中子数为4.0NA | |
| D. | 2.4g Mg在足量O2中燃烧,转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol稀硫酸和1 mol稀Ba(OH)2溶液完全中和所放出的热量为中和热 | |
| B. | 中和反应都是放热反应,多数分解反应是吸热反应 | |
| C. | 在101 kPa时,1 mol碳燃烧所放出的热量一定是碳的燃烧热 | |
| D. | 碳与二氧化碳的反应既是放热反应,也是化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com