
| n |
| V |
| 12.1g |
| 56g/mol+65g/mol |
| 0.1mol×2+0.1mol×2 |
| 2 |
| 0.1mol |
| 0.5L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、酒精在实验台上燃烧时,用水扑灭火焰 |
| B、给试管中的液体加热时,试管口不能对着别人 |
| C、大量有毒易燃气体在室内扩散,应立即打开排气扇开关 |
| D、不慎将浓硫酸沾到皮肤上,应用较多的水冲洗,然后涂上硼酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
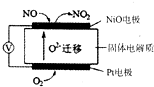 NO2是汽车尾气中的主要污染物之一.
NO2是汽车尾气中的主要污染物之一.
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径大小关系是Xn-<Yn+ |
| B、Z一定是稀有气体元素的原子 |
| C、原子序数关系是Z>Y>X |
| D、原子半径关系是Y<X |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y、Z、R的简单离子具有相同的电子层结构 |
| B、X、Z分别与Y均可形成A2B与A2B2型化合物,且A2B2均有较强的氧化性 |
| C、X2Y分子同存在氢键,故X2Y比X2W稳定 |
| D、由X、Y、Z形成的化合物能与X、Y、R形成的化合物发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
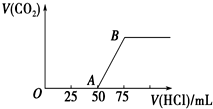 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示.
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、1.5mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物理性质 | 易溶于水,不溶于乙醇;熔点 48.2℃;在潮湿的空气中易潮解 |
| 化学性质 | 43℃以上的空气中易风化;遇酸易分解 (S2O32-+2H+=S↓+SO2↑+H2O ) |
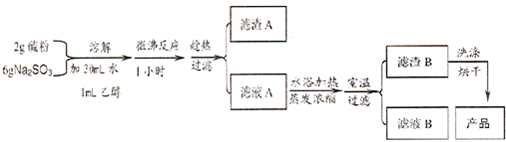
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com