
【题目】某反应中反应物与生成物有![]() 、
、![]() 、
、![]() 、Cu。
、Cu。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:

①图中X溶液的溶质是______________________;
②Cu电极上发生的电极反应式为_________________;
③原电池工作时,盐桥中的_______________离子![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() 不断进入X溶液中。
不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是___________极;
②图丙中的②线是_______________离子的变化。
③当电子转移为2mol时,向乙烧杯中加入_________![]() 溶液才能使所有的金属阳离子沉淀完全。
溶液才能使所有的金属阳离子沉淀完全。
【答案】![]() 、
、![]()
![]()
![]() 负
负 ![]()
![]()
【解析】
(1)根据所给物质,能发生氧化还原反应的是Cu+2Fe3+=2Fe2++Cu,装置甲为电池,溶液X为FeCl3和FeCl2,以及原电池工作原理,据此分析;
(2)根据丙图可知溶液中有三种金属阳离子,而根据X的成分可知X中只有两种金属阳离子,说明在电解过程中还有Cu2+生成,Cu作阳极,石墨作阴极,据此分析;
(1)①甲为电池,发生氧化还原反应,据反应物和生成物可以确定该反应为![]() , X为
, X为![]() 、
、![]() 溶液;
溶液;
答案为:![]() 、
、![]() ;
;
②根据①的分析,Cu为负极,Cu电极上发生的电极反应式为:![]() ;
;
答案为:![]() ;
;
③原电池工作时,电解质溶液中阳离子移向正极,阴离子移向负极,石墨为正极,盐桥中的![]() 离子不断进入X溶液中;
离子不断进入X溶液中;
答案为:![]() ;
;![]()
(2)①根据丙图可知溶液中有三种金属阳离子,而根据X的成分可知X中只有两种金属阳离子,说明在电解过程中还有![]() 生成,因此Cu作阳极,石墨作阴极,所以M是负极;
生成,因此Cu作阳极,石墨作阴极,所以M是负极;
答案为:负;
②根据丙图可知溶液中有三种金属阳离子,根据转移电子的物质的量和金属阳离子的物质的量的变化,可知①为![]() ,②为
,②为![]() ,③为
,③为![]() ;
;
答案为:![]() ;
;
②当电子转移为2mol时,溶液中有![]() ,
,![]() ,
,![]() 为1mol,所以需要加入NaOH溶液14mol,所以NaOH溶液等体积为
为1mol,所以需要加入NaOH溶液14mol,所以NaOH溶液等体积为![]() ;
;
答案为:![]() 。
。


 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】已知 H2(g) + Cl2 (g)===2HCl(g) Δ H =- 184.6 kJ · mol-1则反应:HCl(g)===1/2H2(g)+1/2Cl2(g)的ΔH 为( )
A.+184.6 kJ·mol-1B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1D.+92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是主要大气污染物之一,工业上可用如下装置吸收转化SO2(A、B为惰性电极)。下列说法正确的是
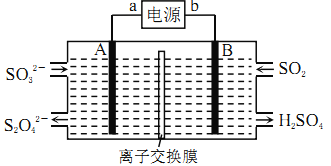
A. 电子流动方向为:B→b→a→A
B. a、A极上均发生氧化反应
C. 离子交换膜为阳离子交换膜
D. B极上的电极反应式为:SO2+2eˉ+2H2O=SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中,有广泛应用,它的工作原理如下:Cd+2NiO(OH)+2H2O ![]() Cd(OH)2+2Ni(OH)2.下列叙述正确的是
Cd(OH)2+2Ni(OH)2.下列叙述正确的是
A. 该电池放电的时候,负极附近pH增大
B. 放电时每转移2mol电子,有2mol NiO(OH)被氧化
C. 充电时,阳极反应式是Ni(OH)2-e-+OH-=NiO(OH)+H2O
D. 充电时,Cd电极接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置的说法中正确的是( )
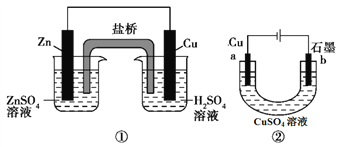
A. 装置①中,盐桥中的Cl- 移向H2SO4溶液
B. 装置②工作一段时间后,可加适量的Cu(OH)2恢复原溶液(原CuSO4溶液足量)
C. 装置①②中的溶液内的H+都在铜电极上被还原,有气泡产生
D. 装置②工作一段时间后,b极附近溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molFeCl3完全水解生成的Fe(OH)3胶粒数为0.1NA
B.0.1mol/LNa2SO3溶液中离子总数大于0.3NA
C.电解精炼铜时,阴极增重3.2g,电路中转移电子数为0.1NA
D.将0.1molO2与0.2molNO在密闭容器中允分反应,反应后容器内分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)配制![]() 溶液时为防止其水解,可加入少量________。用离子方程式表示
溶液时为防止其水解,可加入少量________。用离子方程式表示![]() 可作净水剂的原因__________________________________。
可作净水剂的原因__________________________________。
(2)常温下,pH均为11的氢氧化钠溶液和硫化钠溶液中,水电离出的![]() 浓度之比为________。向硫化钠溶液中加入氯化铝时,产生白色沉淀和臭鸡蛋气味的气体,反应的离子方程式为_______________________________________________。
浓度之比为________。向硫化钠溶液中加入氯化铝时,产生白色沉淀和臭鸡蛋气味的气体,反应的离子方程式为_______________________________________________。
(3)在![]() 时,有pH为a的盐酸和pH为b的NaOH溶液,取
时,有pH为a的盐酸和pH为b的NaOH溶液,取![]() 该盐酸,同该NaOH溶液恰好中和,需
该盐酸,同该NaOH溶液恰好中和,需![]() 溶液。若
溶液。若![]() ,则
,则![]() _________。
_________。
(4)用石墨作电极,在![]() 、
、![]() 、
、![]() 、
、![]() 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
①当阴极放出![]() ,阳极放出
,阳极放出![]() 时,电解质是________。
时,电解质是________。
②当阴极析出金属,阳极放出![]() 时,电解质是________。
时,电解质是________。
③当阴极放出![]() ,阳极放出
,阳极放出![]() 时,电解质是________。
时,电解质是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,常温下甲、丙、丁均可与乙反应生成盐和水,X、Z、W的原子序数及0.1 mol/L甲、丙、丁溶液的pH如图所示(已知lg2=0.3)。下列说法正确的是
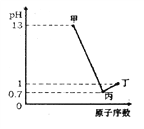
A. 简单阴离子的还原性:Z<W
B. X、Y分别与W形成的化合物皆为离子化合物
C. 乙固体中加入甲的溶液或浓氨水,固体都能溶解
D. Y、Z的简单离子都会影响水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富铁铝土矿![]() 主要含有
主要含有![]() 、
、![]() 、FeO和
、FeO和![]() 可制备新型净水剂液体聚合硫酸铝铁
可制备新型净水剂液体聚合硫酸铝铁![]() 研究发现,当
研究发现,当![]() 时净水效果最好.工艺流程如下
时净水效果最好.工艺流程如下![]() 部分操作和产物略
部分操作和产物略![]() :
:
![]()
![]() 与
与![]() 发生反应的离子方程式是 ______ .
发生反应的离子方程式是 ______ .
![]() 测得滤液中
测得滤液中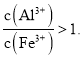 加入
加入![]() 和
和![]() 的作用是
的作用是![]() 结合化学用语说明
结合化学用语说明![]() ______ .
______ .
![]() 将溶液A电解得到液体聚合硫酸铝铁.装置如图所示
将溶液A电解得到液体聚合硫酸铝铁.装置如图所示![]() 阴离子交换膜只允许阴离子通过,电极为惰性电极
阴离子交换膜只允许阴离子通过,电极为惰性电极![]()
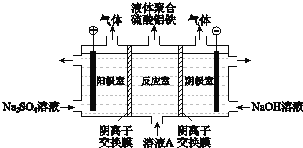
![]() 阴极室的电极反应式是 ______ .
阴极室的电极反应式是 ______ .
![]() 电解过程阳极室溶液pH的变化是 ______
电解过程阳极室溶液pH的变化是 ______ ![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() .
.
![]() 简述在反应室中生成液体聚合硫酸铝铁的原理 ______ .
简述在反应室中生成液体聚合硫酸铝铁的原理 ______ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com