
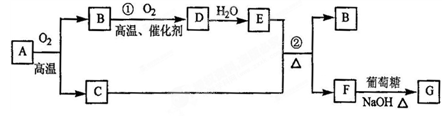
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。 2SO3,平衡时生成三氧化硫是0.12mol,则消耗SO2和氧气分别0.12mol和0.06mol,剩余SO2和氧气分别是0.11mol和0.05mol,所以平衡常数为
2SO3,平衡时生成三氧化硫是0.12mol,则消耗SO2和氧气分别0.12mol和0.06mol,剩余SO2和氧气分别是0.11mol和0.05mol,所以平衡常数为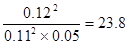 。增大氧气浓度,平衡向正反应方向移动,SO2的浓度减小,氧气的转化率减小。原平衡中三氧化硫的体积分数为
。增大氧气浓度,平衡向正反应方向移动,SO2的浓度减小,氧气的转化率减小。原平衡中三氧化硫的体积分数为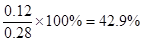 。如果再加入0.5mol氧气,则三氧化硫最多生成0.23mol。其体积分数为
。如果再加入0.5mol氧气,则三氧化硫最多生成0.23mol。其体积分数为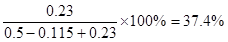 ,所以三氧化硫的体积分数减小。
,所以三氧化硫的体积分数减小。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.原子核外M层有8个电子的元素 |
| B.原子核外L层比M层多一个电子的元素 |
| C.最高价为+7价的元素 |
| D.无负化合价的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
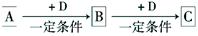
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
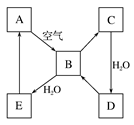
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
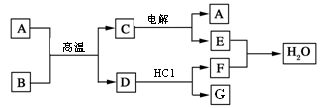
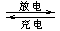 NaCl +D
NaCl +D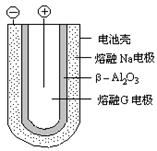
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
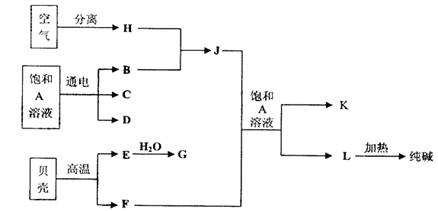
|
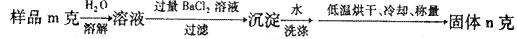
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
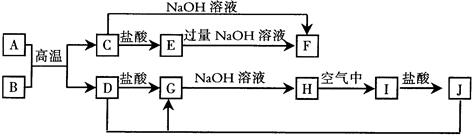
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com