
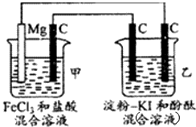
| A、甲池中Mg极为阳极,电极反应式为:Mg-2r-═Mg2+ |
| B、甲池中:当Mg减少2.4g时,石墨(C)极上产生2.24L气体 |
| C、乙池中将化学能转化为电能 |
| D、乙池左侧石墨电极附近变蓝,右侧石墨电极附近变红 |


科目:高中化学 来源: 题型:
| A、向某FeCl2溶液中加入Na2O2粉末,出现红褐色沉淀,说明原FeCl2溶液已氧化变质 |
| B、取少量溶液X,加入适量新氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C、粗略配制2mol?L-1的NaCl溶液,称58.5g NaCl,加入到盛有500mL水的烧杯中,搅拌、溶解 |
| D、溶液X中通入足量CO2,未看到白色沉淀,则说明原溶液中一定不存在大量Ca2+或Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| D、晶体中一定存在化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
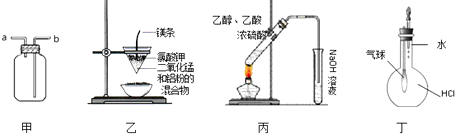
| A、装置甲:气体从a口进入,收集NH3 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.65 | B、0.72 |
| C、1.00 | D、1.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示反应进行过程中气体平均相对分子质量的变化 |
B、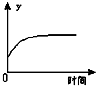 表示反应进行过程中气体密度的变化 |
C、 表示反应达到平衡后,移去一些焦炭后水蒸气的百分含量的变化(忽略表面积的影响) |
D、 表示反应达到平衡后,升高温度CO的百分含量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| ||

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com