
| c(H+) |
| c(F-) |
| A、变大 | B、变小 |
| C、不变 | D、无法确定 |
| c(H+) |
| c(F-) |


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
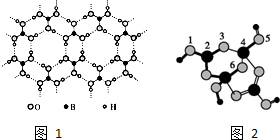 硼酸晶体具有层状结构,每一层的结构结构如图1所示.
硼酸晶体具有层状结构,每一层的结构结构如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 gCH4与18 gNH4+所含质子数相等 |
| B、CH4O和C2H6O都符合CnH2n+2O的通式,它们可能互为同系物 |
| C、32S与33S的质子数相等,属于同一种元素的不同原子 |
| D、质量相等、体积不等的N2和C2H4的分子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是七个基本物理量之一 |
| B、氮气的摩尔质量是28g |
| C、0.5mol氢气的体积为11.2L |
| D、1molH2O约含有6.02×1023个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水加热到很高的温度都难以分解 |
| B、水结成冰体积膨胀,密度变小 |
| C、CH4、SiH4、GeH4、SnH4熔点递增 |
| D、乙醇能与水任意比例互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Kw值随温度升高而增大 |
| B、纯水中,25℃时,c(H+)?c(OH-)=1×10-14 |
| C、25℃时,任何以水为溶剂的稀溶液中c(H+)?c(OH-)=1×10-14 |
| D、蒸馏水中,c(H+)?c(OH-)=1×10-14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com