
【题目】向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式_____________________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是______(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的__________曲线表示(填序号)。
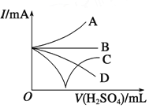
【答案】 Ba2++2OH-+SO42-+2H+===BaSO4↓+2H2O A C
【解析】(1)氢氧化钡与硫酸反应生成硫酸钡沉淀和水;
(2)根据反应物和生成物书写相应的离子方程式,然后与(1)对比即可;
(3)加入稀硫酸直至过量,恰好反应时导电性近乎为0,过量后离子浓度增大,导电性增强。
(1)向Ba(OH)2溶液中逐滴加入稀硫酸发生中和反应生成硫酸钡和水,离子方程式为Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O;
(2)A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,生成硫酸钡、硫酸钠和水,反应的离子方程式为Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O,A正确;
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,生成硫酸钡、氢氧化钠和水,反应的离子方程式为Ba2++OH-+SO42-+H+=BaSO4↓+H2O,B错误;
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,生成硫酸钡、氢氧化钠和水,反应的离子方程式为Ba2++OH-+SO42-+H+=BaSO4↓+H2O,C错误;
答案选A。
(3)若缓缓加入稀硫酸直至过量,恰好反应时生成硫酸钡沉淀和水,导电性近乎为0,过量后离子浓度增大,导电性增强,图中只有C符合。
答案选C。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】为确定混合均匀的NH4NO3和(NH4)2SO4样品组成,称取4份样品分别加入50.0mL相同浓度的NaOH溶液中,加热充分反应(溶液中的铵根离子全部转化为氨气,且加热后氨气全部逸出).加入的混合物的质量和产生的气体体积(标准状况)的关系如表:
实验序号 | I | II | III | IV |
NaOH溶液的体积(mL) | 50.0 | 50.0 | 50.0 | 50.0 |
样品质量(g) | 3.44 | m | 17.2 | 21.5 |
NH3体积(L) | 1.12 | 2.24 | 5.60 | 5.60 |
试计算:
(1)m=_____g;c(NaOH)=_____molL﹣1。
(2)样品中NH4NO3和(NH4)2SO4物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如图所示装置,测定工业纯碱(含有少量NaCl)中Na2CO3的含量.

(1)检验装置B气密性:塞紧三孔橡胶塞,夹紧弹簧夹,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________________,说明装置不漏气.
(2)装置A的作用是____,装置C中的试剂为___.
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?____(选填“必要”或“不必要”),判断的理由是____________________.
(4)实验前称取28.80g样品,实验后D装置增重8.80g,则样品中Na2CO3质量分数为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. Cl2通入水中:Cl2 + H2O![]() H+ + Cl-+HClO
H+ + Cl-+HClO
B. CaCO3加入醋酸中:CO![]() + 2H+ = CO2↑ + H2O
+ 2H+ = CO2↑ + H2O
C. 用惰性电极电解MgCl2溶液:2Cl-+2H2O ![]() H2↑+ Cl2↑ +2OH-
H2↑+ Cl2↑ +2OH-
D. 酸性KMnO4溶液滴入FeSO4溶液中:MnO![]() + Fe2+ + 8H+ = Mn2+ + Fe3+ + 4H2O
+ Fe2+ + 8H+ = Mn2+ + Fe3+ + 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
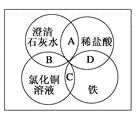
A. OH-+HCl===H2O+Cl-
B. Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C. Fe+Cu2+===Cu+Fe2+
D. Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】L多巴胺是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下

下列关于L多巴胺的叙述不正确的是( )
A. 它属于α氨基酸,既具有酸性,又具有碱性
B. 它遇到FeCl3溶液显紫色
C. 它可以两分子间缩合形成分子式为C18H18O6N2的化合物,该化合物中有3个六元环
D. 它既与酸反应又与碱反应,等物质的量的L多巴胺最多消耗NaOH与HCl的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下甲胺(CH3NH2)的电离常数kb,pkb=-lgkb=3.4。CH3NH2+H2O![]() CH3NH3++OH-。下列说法不正确的是( )
CH3NH3++OH-。下列说法不正确的是( )
A. (CH3NH3)2SO4溶液中离子浓度:c(CH3NH3+)>c(SO42-)>c(H+)>c(OH-)
B. 常温下,pH=3的盐酸溶液和pH=11的CH3NH2溶液等体积混合,混合溶液呈酸性
C. 用标准浓度的盐酸滴定未知浓度的CH3NH2溶液的实验中,选择甲基橙作指示剂
D. 常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=10.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,设计正确且能达到实验目的的是
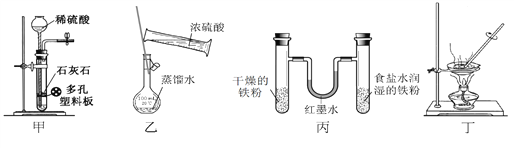
A. 甲用于实验室制取少量CO2 B. 乙用于配制一定物质的量浓度的硫酸
C. 丙用于模拟生铁的电化学腐蚀 D. 丁用于蒸干A1Cl3溶液制备无水AlC13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述或书写正确的是
A. 2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1,则1mol氢气的燃烧热大于241.8 kJ·mol-1
B. H2(g)+F2(g)=2HF(g)ΔH=-270kJ·mol-1,则相同条件下,2molHF气体的能量大于1mol氢气和1mol 氟气的能量之和
C. 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该中和反应的热化学方程式为NaOH+HCl=NaCl+H2OΔH=-57.4kJ·mol-1
D. 500℃、30MPa时,发生反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1。在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ
2NH3(g) ΔH=-38.6kJ·mol-1。在此条件下将1.5molH2和过量N2充分反应,放出热量19.3kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com