
分析 设平衡时转化Bxmol,则
2A(g)+B(g)?2C(g)
起始(mol) 4 2 0
转化(mol) 2x x 2x
平衡(mol)4-2x 2-x 2x
平衡时C的体积分数为40%,可计算x值,以此可计算平衡常数、反应速率以及转化率.
解答 解:设平衡时转化Bxmol,则
2A(g)+B(g)?2C(g)
起始(mol) 4 2 0
转化(mol) 2x x 2x
平衡(mol)4-2x 2-x 2x
平衡时C的体积分数为40%,则$\frac{2x}{6-x}×100%$=40%,x=1,
(1)该温度下此反应的平衡常数$\frac{(\frac{1}{4})^{2}}{(\frac{2}{4})^{2}(\frac{1}{4})}$=1,答:此反应的平衡常数为1;
(2)反应开始至平衡时B的反应速率为$\frac{\frac{1mol}{4L}}{50s}$=0.005mol/L(L•s),
答:B的反应速率为0.005mol/L(L•s);
(3)达到平衡时A的转化率为$\frac{2}{4}×100%$=50%,
答:达到平衡时A的转化率为50%.
点评 本题考查化学平衡的计算,为高考常见题型,侧重考查学生的分析、计算能力,注意三段式解答方法的利用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入足量稀盐酸无沉淀,再加入氯化钡溶液后有白色沉淀产生,一定有SO42- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 某溶液中加入硝酸银溶液生成白色沉淀,说明溶液中有Cl- | |
| D. | 无色溶液中加入稀盐酸产生无色气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
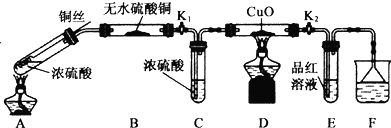
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
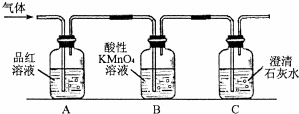
 硫酸是常用的化学试剂和重要的化工原料.实验室中我们用浓硫酸做过如下实验.
硫酸是常用的化学试剂和重要的化工原料.实验室中我们用浓硫酸做过如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75% | B. | 50% | C. | 25% | D. | 20% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
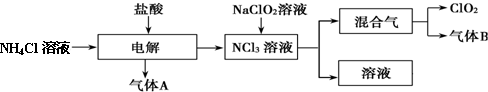
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
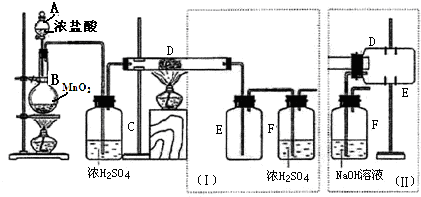
| 可能影响因素 | 实验操作 | 预期现象和结论 |
| ①溶液的酸性 | 取少量0.5mol•L-1Fe(NO3)3于试管中,加入几滴3.0mol•L-1HNO3. | 现象:棕黄色溶液颜色变浅; 结论:酸性增强抑制Fe3+水解. |
| ②溶液的浓度 | 取10mL0.5mol•L-1 Fe(NO3)3于烧杯中,用pH计测得pH1.另取90mL蒸馏水加入烧杯,充分搅拌,再测得pH2. | 现象:pH2-pH1<1(或正确表达) 结论:稀释促进水解(或平衡右移) |
| ③溶液的温度 | 取少量0.5mol•L-1Fe(NO3)3于试管中,用酒精灯加热一段时间,观察溶液颜色 | 现象:加热后溶液颜色变深 结论:升高温度促进Fe3+水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com