
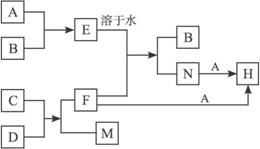
(1)写出有关反应的离子方程式:
E的水溶液+F:_______________________________________________________。
A+N:_______________________________________________________________。
M对应的氢氧化物与氢氧化钠溶液反应:_________________________________。
C+D:(写出化学方程式)______________________________________________。
(2)在足量的稀N溶液中,加入少量A的水溶液,振荡后溶液变为黄绿色。甲同学认为这不是发生化学反应所致,是A水溶液的颜色,乙同学认为这是发生化学反应所致,使溶液变黄绿色的物质是生成物和A水溶液的混合颜色。
①请你判断哪位同学的推断是正确的?_____________(填“甲”或“乙”)。
②请你设计一个实验探究你的判断(要求写出化学实验必要的操作步骤,所用化学试剂及实验现象,以及得出的化学实验结论)。
(1)Fe+2H+====Fe2++H2↑
2Fe2++Cl2====2Fe3++2Cl-
Al(OH)3+OH-====![]() +2H2O
+2H2O
2Al+Fe2O3![]() Al2O3+2Fe
Al2O3+2Fe
(2)①乙 ②取少量的稀N溶液加入试管中,向试管中滴加KSCN溶液,没有变化,再滴加A的溶液,试管中混合液变血红色,溶液中的Fe2+被氧化生成Fe3+,Fe3+与SCN-结合生成血红色物质。
解析:本题考查了元素化合物知识并结合实验设计。此题的题眼是化学反应特点以及反应类型的辨别。由A、B、C、F为单质可知其中有两个置换反应,有两个氧化还原反应。而且一种单质气体具有强氧化性,所以可推测为Cl2。另外的化合价发生变化的金属元素应该为Fe。根据其他的反应得:A—Cl2、B—H2、C—Al、D—Fe2O3、E—HCl、F—Fe、N—FeCl2、M—Al。


科目:高中化学 来源: 题型:
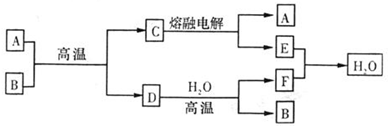
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013届新疆乌鲁木齐八中高三第一次月考化学试卷(带解析) 题型:填空题
(8分)如图所示,已知A、D、E、F是中学常见的单质,B、C是氧化物,且B是红棕色固体,请填空: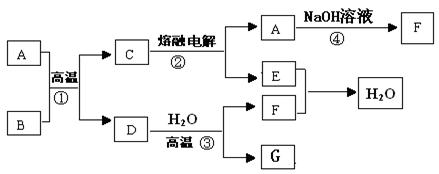
(1)A 是 , B是 。(填化学式)
(2)写出反应③的化学方程式为 。
(3)写出反应④的化学方程式为 。
(4)C电解时,每生成1molA ,同时生成 molE。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年新疆乌鲁木齐八中高三第一次月考化学试卷(解析版) 题型:填空题
(8分)如图所示,已知A、D、E、F是中学常见的单质,B、C是氧化物,且B是红棕色固体,请填空:
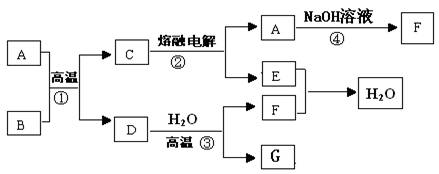
(1)A 是 , B是 。(填化学式)
(2)写出反应③的化学方程式为 。
(3)写出反应④的化学方程式为 。
(4)C电解时,每生成1molA ,同时生成 molE。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、F是中学化学常见的单质,在相同条件下,气体A的密度大于气体B的密度,D为红棕色固体。其有关转化如下:

(1)①写出A与N反应的离子方程式 。
②写出C与D反应的化学方程式 。
(2)怎样检验N溶液中的阳离子,简述实验步骤 。
(3)将H的水溶液加热蒸干并灼烧,得到的固体为 (写化学式),其有关反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com