
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图,下列说法正确的是()
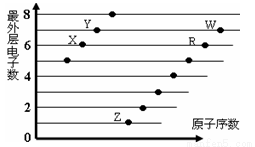
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:Y>X
D.X、Z形成的化合物中只有离子键
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高一下6月考化学卷(解析版) 题型:选择题
下列反应产物不受反应条件不同而影响的是 ( )
A.甲苯与溴蒸汽的反应 B. H2和Cl2反应
C. 乙烯与氧气的反应 D. 乙酸乙酯的水解
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三5月适应性训练理综化学试卷(解析版) 题型:实验题
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等。
(1)其制备方法为:
(2)已知:①
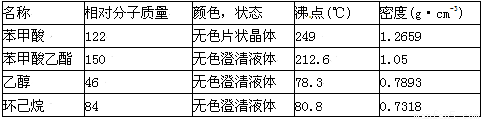
②苯甲酸在100℃会迅速升华
③无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
(3)实验步骤如下:
① 在仪器A中加入12.20 g苯甲酸,25 mL 9 5%的乙醇(过量),20 mL环己烷以及4 mL浓硫酸,混合均匀并加入沸石,按下图所示装好仪器,控制温度在65~70℃加热回流2 h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
5%的乙醇(过量),20 mL环己烷以及4 mL浓硫酸,混合均匀并加入沸石,按下图所示装好仪器,控制温度在65~70℃加热回流2 h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
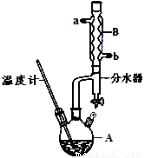
② 反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③ 将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继 续升温,接收210~213℃的馏分。
续升温,接收210~213℃的馏分。
④ 检验合格,测得产品体积为12.86 mL。回答下列问题:
(1)在该实验中,仪器A的名称为 ,其容积最适合的是 (填选项前的字母)。
A.25 mL B.50 mL C.100 mL D.250 mL
(2)制备苯甲酸乙酯时,最合适的加热方法是 ,控制温度的目的是 。加入沸石的作用是 。
(3)步骤①中使用分水器不断分离除去水的目的是 。
(4)步骤②中应控制馏分的温度在 。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(5)步骤③有机层应从分液漏斗 (填“上口”或“下口”)流出。加入Na2CO3的作用是 ;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是 。加入氯化钙的目的是 。
(6)计算本实验的产率为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
在塑料袋中放一个成熟的苹果,再放些青香蕉,将袋口密封。两天后,发现青香蕉成熟了。导致青香蕉成熟的物质是成熟苹果释放出的
A.C6H6 B.CH3COOH C.C2H4 D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
结构简式为 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)()
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)()
A.4种 B.5种 C.6种 D.7种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
已知氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列有关叙述中不正确的是()
①NH4H是离子化合物,含有离子键和共价键 ②NH4H溶于水所形成的溶液显酸性
③NH4H与水反应时,NH4H是氧化剂 ④NH4H固体投入少量的水中,有两种气体产生
A.①② B.②③ C.①②③ D.全部
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
低合金高强度钢Q460是支撑“鸟巢”的铁骨钢筋,除含有铁元素外,还含有Mn(锰)、Ti(钛)、Cr(铬)、Nb(铌)等合金元素,下列有关说法正确的是( )
A.Fe位于元素周期表的第四周期、第ⅧB族
B.工业上利用热还原法冶炼金属Fe、Cr、Mn
C.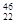 TiO2、
TiO2、 TiO2、
TiO2、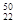 TiO2互为同位素
TiO2互为同位素
D.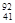 Nb3+原子核内有51个中子,核外有41个电子
Nb3+原子核内有51个中子,核外有41个电子
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市高三高考前最后一卷理综化学试卷(解析版) 题型:实验题
二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质)。某课题小组以此粉末为原料设计资源回收的工艺流程如下:
 (1)写出第①步反应的离子方程式 。
(1)写出第①步反应的离子方程式 。
(2)洗涤滤渣B的目的是为了除去 (填离子符号),检验该离子是否洗净的方法是 。
(3)写出第③步反应的化学方程式_________________________。
(4)制备绿矾(FeSO4·7H2O)时,向Fe2(SO4)3溶液中加入过量铁屑,充分反应后,经过滤得
到FeSO4溶液,再经 、 、过滤、洗涤、干燥等操作步骤得到绿矾。
(5)取上述流程中得到的Ce(OH)4产品(质量分数为80.00%)1.300g,加硫酸溶解后,用0.1000mol/L FeSO4溶液滴定至终点(铈被还原成Ce3+),则需准确滴加标准溶液的体积为 mL。
(可能用到的相对原子质量 H=1 O=16 Ce =140 )
②该电解反应的化学方程式为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com