

| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
| 1mol |
| 1mol/L |
| 3mol |
| 1L |
| 0.75×0.75 |
| 0.25×0.753 |


科目:高中化学 来源: 题型:
| A、NH4HCO3和盐酸的反应是放热反应 |
| B、该反应中,热能转化为产物内部的能量 |
| C、反应物的总能量高于生成物的总能量 |
| D、反应的热化学方程式为NH4HCO3+HCl-→NH4Cl+CO2↑+H2O△H=+Q kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离出的c(OH-)=1×10-6 mol/L |
| B、c(Na+)=c(X-)+c(HX) |
| C、c(Na+)-c(OH-)=c(X-)-c(H+) |
| D、c(X-)=c(Na+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验事实 | 结论 | |
| A. | 氯水可以导电 | 氯气是电解质 |
| B. | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C. | 乙烯能使KMnO4溶液褪色 | 乙烯具有还原性 |
| D. | 将SO2通入含HClO的溶液中,生成H2SO4 | 说明HClO酸性比H2SO4 强 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
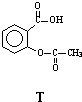
| A、T可以发生酯化反应 |
| B、T可以与NaOH溶液反应 |
| C、T属于芳香烃类化合物 |
| D、T在酸中水解可以得到CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、振荡试管中的液体时,应用手指拿住试管,左右摆动手腕振荡试管 |
| B、在做蒸馏实验时要加入少量的碎瓷片,以防止溶液暴沸 |
| C、如果皮肤上不慎沾上浓硫酸,应立即用大量的NaOH稀溶液冲洗 |
| D、用石蕊或酚酞试纸进行气体验满时,最好先用蒸馏水湿润 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com