
根据原子结构及元素周期律的知识,下列推断正确的是( )
A. Cl与Cl得电子能力相同
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.同主族元素含氧酸的酸性随核电荷数的增加而减弱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
一定温度下,对于反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施能增大反应速率的是 ( )。
2NO(g)在密闭容器中进行,下列措施能增大反应速率的是 ( )。
A.降低温度 B.恒容充入氮气 C.恒压充入氦气 D.恒容充入氦气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高二下期中化学试卷(解析版) 题型:选择题
如图所示,Na?S电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
2Na(l)+S8(l)  Na2Sn。下列说法不正确的是
Na2Sn。下列说法不正确的是

A.外室熔融硫中添加石墨粉主要是为了增强导电性
B.放电时Na+向正极移动
C.充电时阳极反应式为8S-16e-===nS8
D.充电时钠极与外接电源的正极相连
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高一下期中化学A卷(解析版) 题型:选择题
( )下列说法正确的是
A.在化学反应中某元素由化合态变为游离态,该元素一定被还原了
B.失电子难的原子其得电子的能力一定强
C.电子层结构相同的各种离子,它们的半径随核电荷数的增加而减小
D.最外层电子数较少的金属元素,一定比最外层电子数较它多的金属元素活泼
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高一下期中化学A卷(解析版) 题型:选择题
( )下列分子中所有原子都满足最外层8电子稳定结构的是
A.五氯化磷(PCl5) B.次氯酸(HClO)
C.二氧化碳(CO2) D.三氟化硼(BF3)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:填空题
(物质结构与质性题)X、Y、Z、W是元素周期表前四周期中常见的元素,原子序数依次增大。其相关信息如下表:
元素 | 相关信息 |
X | X的基态原子价层电子中有两个未成对电子 |
Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
Z | Z存在质量数为23,中子数为12的核素 |
W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)X的电负性比Y的________(填“大”或“小”);
X 和Y的气态氢化物中,较稳定的是 (写化学式)。
(2)W在周期表中的位置是 ,其基态原子价电子的电子排布式为 。
(3)Z2Y2的电子式为 ,请写出Z2Y2与XY2反应的化学方程式 。
(4)在XY2分子中X原子的杂化方式为 ,其分子的空间构型为 。氢、X、Y三种元素可共同形成多种分子和一种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
只用一种试剂就能将甲苯、环己烯、四氯化碳、碘化钾溶液区分开来,该试剂可以是
A.溴化钾溶液 B.溴水 C.高锰酸钾溶液 D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二下期中化学试卷(解析版) 题型:选择题
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂一KNO3的U型管)构成—个原电池。以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极;②正极反应为:Ag++e-=Ag;
③实验过程中取出盐桥,原电池仍继续工作;④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.①② B.②④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期中化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g)△H1=—99kJ.mol-1,
CH3OH(g)△H1=—99kJ.mol-1,
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
CH3OH(g)+H2O(g)△H2=—58kJ.mol-1
③CO2(g)+H2(g) CO(g)+H2O(g)△H3
CO(g)+H2O(g)△H3
回答下列问题:
(1)写出CO2的结构式__________。
(2)由上述数据计算出△H3=kJ.mol-1
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,温度T1、T2对反应的影响,下列正确的是__________(填序号)
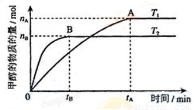
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tAmol/(L·min)
②该反应在T1时的平衡常数比T2时的小
③当生成1mol甲醇的同时,生成1molCO2,说明反应达到平衡
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;该温度条件下,反应平衡常数为__________(计算出结果)
(5)在直接以甲醇为燃料电池中,电解质溶液为硫酸性,负极的电极反应式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com