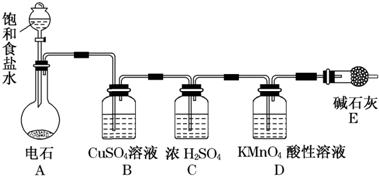
为测定乙炔的相对分子质量,某小组利用如图所示装置进行试验(夹持仪器已略去,气密性已检验).
(1)小组查阅资料得出:乙炔能与硫酸酸化的KMnO
4反应生成Mn
2+和CO
2,该反应的化学方程式是
C2H2+2KMnO4+3H2SO4═K2SO4+2MnSO4+2CO2↑+4H2O
C2H2+2KMnO4+3H2SO4═K2SO4+2MnSO4+2CO2↑+4H2O
.
(2)在装置A中使用饱和食盐水而不直接滴加水的原因
为了减缓电石与水的反应速率
为了减缓电石与水的反应速率
.
(3)B中的CuSO
4溶液用于除去乙炔中混有的H
2S、PH
3、AsH
3等气体,CuSO
4溶液除H
2S气体的反应类型是
复分解反应
复分解反应
(基本反应).
(4)实验前D中含有x mol KMnO
4的酸性溶液,实验时向D中通入一定量的乙炔直至KMnO
4酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重y g,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):
(不写计算过程).
(5)若该小组的实验原理及所有操作都正确,下列因素中,对所测乙炔相对分子质量的值不会产生影响的是
C
C
.
A.将装置A中产生的混合气体直接通入D中的KMnO
4酸性溶液
B.将E装置(盛有碱石灰的干燥管)换成盛有浓硫酸的洗气瓶
C.通入过量纯净的乙炔气体于KMnO
4酸性溶液时,有部分乙炔未被氧化而逸出
(6)另一活动小组的同学认为上述实验装置仍存在不足,则改进的措施是
在E装置后面再接一个盛有碱石灰的干燥管
在E装置后面再接一个盛有碱石灰的干燥管
.




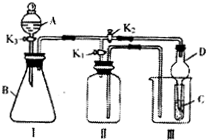 某小组设计如图装置:可用于制取多种气体,也可用于验证物质的性质.
某小组设计如图装置:可用于制取多种气体,也可用于验证物质的性质.