
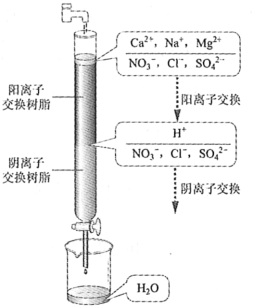
【题目】离子交换法净化水过程如图所示。下列说法中错误的是
A. 经过阳离子交换树脂后,水中阳离子的总数不变
B. 水中的![]() 、
、![]() 、Cl通过阴离子树脂后被除去
、Cl通过阴离子树脂后被除去
C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH![]() H2O
H2O
【答案】A
【解析】
离子交换树脂净化水的原理是:当含有Na+、Ca2+、Mg2+等阳离子及SO42-、Cl-、NO3-等阴离子的原水通过阳离子交换树脂时,水中的阳离子为树脂所吸附,而树脂上可交换的阳离子H+则被交换到水中,并和水中的阴离子组成相应的无机酸;当含有无机酸的水再通过阴离子交换树脂时,水中的阴离子也为树脂所吸附,树脂上可交换的阴离子OH-也被交换到水中,同时与水中的H+离子结合成水,则
A、根据电荷守恒可知经过阳离子交换树脂后,水中阳离子总数增加,A错误;
B、根据以上分析可知水中的SO42-、Cl-、NO3-等阴离子通过阴离子交换树脂被除去,B正确;
C、通过净化处理后,溶液中离子的浓度降低,导电性降低,C正确;
D、根据以上分析可知阴离子交换树脂填充段存在反应H++OH-=H2O,D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如下图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
(2)反应III为:CO2(g)+C(s)![]() 2CO(g)
2CO(g) ![]() H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为_________。刻蚀液使用一段时间后会失效,先加酸,再加入过氧化氢溶液,可实现刻蚀液中Fe3+的再生,该反应的离子方程式为_________。
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.将少量饱和氯化铁溶液滴入沸水中,继续煮沸,可制得Fe(OH)3胶体,反应的方程式为:FeCl3 + 3H2O![]() Fe(OH)3(胶体) + 3HCl。
Fe(OH)3(胶体) + 3HCl。
①当溶液呈__时,停止加热,即制得Fe(OH)3胶体。
②氢氧化铁胶体粒子直径大小的范围是________。
③下列叙述错误的是_____。
A.雾属于胶体,能产生丁达尔效应
B.“PM2.5”悬浮在空气中形成胶体,危害人体健康 (“PM2.5”指大气中直径小于或等于2.5微米的细小颗粒物,也可称为可吸入肺颗粒物)
C.明矾、硫酸铁可以净水,净水原理和胶体有关
D.胶体在一定条件下能稳定存在,属于介稳体系
Ⅱ.(1)下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO B. H2、C、P、Cu
C.O2、Fe、Cu、Zn D. HCl、H2O、H2SO4、HNO3
以上四组物质中与其他不同的物质依次是(填化学式):A__;B__;C___;D___。
(2)下列物质:①HCl②蔗糖③NaOH④KCl⑤SO2⑥Fe⑦碳酸钠溶液,属于电解质的是:__(填序号)能导电的是:____(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制备高效漂白剂NaClO2的实验流程如图所示,反应I中发生的反应为3NaClO3+4SO2+3H2O====2ClO2+Na2SO4+3H2SO4+NaCl,下列说法中正确的是
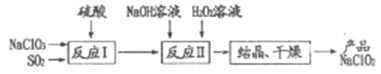
A. 反应Ⅱ中H2O2做还原剂
B. 产品中含有SO42-、Cl-
C. NaClO2的漂白原理与SO2相同
D. 实验室进行结晶操作通常在坩埚中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如图:
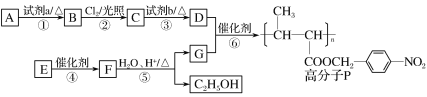
(1)A的分子式是C7H8,其结构简式是_____。
(2)试剂a是____。
(3)反应③的化学方程式:___。
(4)化合物H属于A的同系物,其分子式为C8H10,其同分异构体共有___种,其中___(写结构简式)的一氯代物只有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下的a L NH3完全溶于1 L水,得到体积为V L、密度为b gcm-3(b<1)、物质的量浓度为c molL-1、溶质质量分数为w的氨水(溶质按NH3算 ),下列叙述中错误的是
A.c = ![]()
B.w=![]() ×100%
×100%
C.若将该氨水蒸发出部分水(不考虑溶质NH3的逸出),使溶液质量变为原来一半,则浓度大于2c
D.上述溶液中再加入V L水 ,所得溶液的质量分数小于0.5w
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:H2(g)+1/2O2(g)H2O(g),反应过程中能量变化如图所示,则:

①a、b、c分别代表什么意义?
a______________________________;
b_______________________________;
c_______________________________。
②该反应是ΔH____________0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,已知:H2(g)+![]() O2(g)H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)H2(l) ΔH=-0.92 kJ·mol-1
O2(g)O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝(AlP)是一种常用于粮食仓储的广谱性熏蒸杀虫剂,遇水立即产生高毒性气体PH3(沸点-89.7℃,还原性强)。国家卫计委规定粮食中磷化物(以PH3计)的残留量不超过0.05mg/kg时为质量合格,反之不合格。某化学兴趣小组的同学用下述方法测定某粮食样品中残留磷化物的质量以判断是否合格。

在C中加入100g原粮,E中加入20.00mL2.50×10-4mol/ L KMnO4溶液(H2SO4酸化),往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO4溶液。回答下列问题:
(1)PH3的电子式为___________。仪器D的名称是___________。
(2)通入空气的作用是___________。
(3)装置B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2。若去掉该装置,对实验的影响为___________。
(4)装置E中PH3被氧化成磷酸,则装置E中发生反应的离子方程式为__________。收集装置E中的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10-5mol/L的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液20.00mL,Na2SO3与KMnO4溶液反应的离子方程式为:SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平),则该原粮样品中磷化物(以PH3计)的质量为__________mg。该原粮样品__________(填“合格”或“不合格”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 含有金属元素的化合物一定是离子化合物
B. IA族和VIIA族元素原子化合时,一定生成离子键
C. 由非金属元素形成的化合物一定不是离子化合物
D. 活泼金属与活泼非金属化合时,能形成离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com