
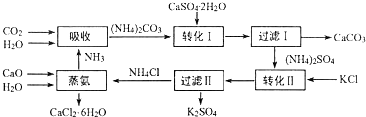
���� ����ͼ���������ջ���NH3��CO2��H2O����̼��泥�̼��狀�ʯ������Һ��Ӧ����CaCO3����NH4��2SO4�������˺���룬��NH4��2SO4��KCl�ı�����Һ�У������ܽ�Ȳ�ͬ������K2SO4���壬���˷���õ�NH4Cl��K2SO4���������ڵ�ΪCaO��H2O��NH4Cl����ΪCaCl2��6H2O��NH3��
��1��������������֪��ԭ�ϳ�CaSO4.2H2O��CaCO3��H2O�⣬����Ҫ������ԭ���ǰ������Ȼ��أ�
̼��狀�ʯ������Һ��Ӧ����CaCO3����NH4��2SO4��
��2������CO32-���ᷴӦ���ɶ�����̼���м��飻
��3������Ksp��CaCO3��=c��Ca2+����c��CO32-�����㣻
��4���������ڵ�ΪCaO��H2O��NH4Cl����ΪCaCl2��6H2O��NH3��
��5���¶ȹ���ʱCaCl2.2H2O��ʧȥ�ᾧˮ���Ȼ��ƽᾧˮ���CaCl2•6H2O����Ŀǰ���õ������Ȳ��ϣ�����Ϊ�Ȼ��ƽᾧˮ�����۵�����ۻ����������������䣬�ܵ����أ�
��� �⣺������ͼ��֪�����ջ���NH3��CO2��H2O����̼��泥�̼��狀�ʯ������Һ��Ӧ����CaCO3����NH4��2SO4�������˺���룬��NH4��2SO4��KCl�ı�����Һ�У������ܽ�Ȳ�ͬ������K2SO4���壬���˷���õ�NH4Cl��K2SO4���������ڵ�ΪCaO��H2O��NH4Cl����ΪCaCl2��6H2O��NH3��
��1��������������֪��ԭ�ϳ�CaSO4.2H2O��CaCO3��H2O�⣬����Ҫ������ԭ����NH3��KCl��
̼��狀�ʯ������Һ��Ӧ����CaCO3����NH4��2SO4����Ӧ���ӷ���ʽΪ��CaSO4+CO32-=CaCO3��+SO42-��
�ʴ�Ϊ��NH3��KCl��CaSO4+CO32-=CaCO3��+SO42-��
��2������CO32-���ᷴӦ���ɶ�����̼���м��飬�������Ϊ��ȡ������Һ���μ�ϡ���ᣬ�������ݲ�������CO32-����֮������CO32-��
�ʴ�Ϊ��ȡ������Һ���μ�ϡ���ᣬ�������ݲ�������CO32-����֮������CO32-��
��3��Ca2+Ũ�ȵ���1.0��10-5mol•L-1 ʱ����Ϊ��������ȫ����ҪʹCa2+������ȫ������Ksp��CaCO3��=c��Ca2+����c��CO32-������֪��Һ��c��CO32-����$\frac{5.0��1{0}^{-9}}{1.0��1{0}^{-5}}$mol/L=5.0��10-4mol/L��
�ʴ�Ϊ��5.0��10-4mol/L��
��4���������ڵ�ΪCaO��H2O��NH4Cl����ΪCaCl2��6H2O��NH3����Ӧ����ʽΪ��CaO+NH4Cl+5H2O$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2��6H2O+2NH3����
�ʴ�Ϊ��CaO+NH4Cl+5H2O$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2��6H2O+2NH3����
��5���¶ȹ���ʱCaCl2.2H2O��ʧȥ�ᾧˮ�������ᾧҪ������160�棻�Ȼ��ƽᾧˮ���CaCl2•6H2O����Ŀǰ���õ������Ȳ��ϣ�����Ϊ�Ȼ��ƽᾧˮ�����۵�ͣ������������ۻ����������������䣬�ܵ����أ�
�ʴ�Ϊ���¶ȹ���ʱCaCl2.2H2O��ʧȥ�ᾧˮ��ad��
���� ���⿼�����ʵ��Ʊ����������������ᴿ���ۺ�Ӧ�ã��ܶȻ��йؼ���ȣ��ؼ������������ԭ�������ط�Ӧԭ���ķ�����Ӧ�ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��Rλ�����ڱ��еڢ�A�� | |
| B�� | Rֻ�ܱ���ԭ | |
| C�� | R2�ڳ��³�ѹ��һ�������� | |
| D�� | ��1mol RO3-����÷�Ӧ����ת�Ƶĵ��ӵ����ʵ���Ϊ5 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɢ�����Ӳ�������ֽ | B�� | ���ж����ЧӦ | ||
| C�� | ��ɢ�ʺܿ�ͳ������� | D�� | ���÷�ɢϵ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
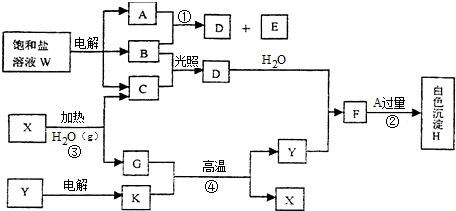
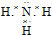 ��B�ľ��������Ƿ��Ӿ��壮
��B�ľ��������Ƿ��Ӿ��壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
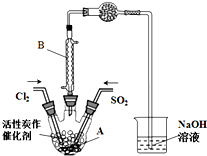 ijѧϰС�����ݷ�Ӧ��SO2��g��+Cl2��g��?SO2Cl2��g����H��0������Ʊ������ȣ�SO2Cl2����װ����ͼ���й���Ϣ�����ʾ��
ijѧϰС�����ݷ�Ӧ��SO2��g��+Cl2��g��?SO2Cl2��g����H��0������Ʊ������ȣ�SO2Cl2����װ����ͼ���й���Ϣ�����ʾ��| SO2Cl2 | Cl2 | SO2 | |
| �۵�/�� | -54.1 | -101 | -72.4 |
| �е�/�� | 69.1 | -34.6 | -10 |
| ���� | ��ˮ���� ����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
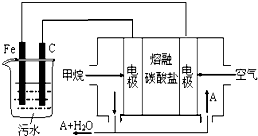
| A�� | FeΪ��������缫��ӦΪ��Fe-3e-+3OH-=Fe��OH��3�� | |
| B�� | ͨ�����ĵ缫Ϊ��������缫��ӦΪ��CH4-8e-+10OH-=CO32-+7H2O | |
| C�� | Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���ع���ʱ���� �в���A���ʲμ�ѭ����A������CO2 | |
| D�� | ʵ������У���������������4.48 L���壬���·��ͨ���ĵ��Ӹ���Ϊ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | T��ʱ��pH=6�Ĵ�ˮ�У����е�OH-��ĿΪ1��10-6NA | |
| B�� | ��״���£�22.4LCCl4�к��еĹ��õ��Ӷ���ĿΪ4.0NA | |
| C�� | 50g98%��Ũ�����У���������ԭ����ĿΪ2NA | |
| D�� | 1molNa2O2������CO2��ַ�Ӧת�Ƶĵ�����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+��H+��SO42-��Cl- | B�� | Na+��Ba2+��NO3-��CO32- | ||
| C�� | Al3+��H+��CO32-��Cl- | D�� | Ba2+��OH-��Fe2+��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������Ӧ�����»�ԭ�ԣ�CO��Pd | |
| B�� | ������Ӧ��PdCl2������ | |
| C�� | �ڱ��������11.2 L CO2ʱ��ת�Ƶĵ���Ϊ2 mo1 | |
| D�� | ������Ӧ��CO2Ϊ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com