
|
ij���淴ӦA(g) | |
| [����] | |
A�� |
���������¶ȱ��������и� |
B�� |
���������¶ȱȼ������и� |
C�� |
��������ʹ���˴��� |
D�� |
��������ʹ���˴��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��ѧϰ�ܱ�����ѧ���˽̿α�߶���(ѡ��4)��2009��2010ѧ�ꡡ��19�ڡ��ܵ�175�� �˽̿α��(ѡ��4) ���ͣ�013
|
ij���淴Ӧ A(g) | |
| [����] | |
A�� |
���������¶ȱ��������и� |
B�� |
���������¶ȱȼ������и� |
C�� |
��������ʹ���˴��� |
D�� |
��������ʹ���˴��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.ƽ��������Ӧ�����ƶ� B.ƽ�ⲻ�����ƶ�
C.���ж�ƽ���ƶ����� D.C�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�����ʡ������һ�и߶���ѧ����ĩ�������ƻ�ѧ�Ծ����������� ���ͣ������
��20�֣�ѡ����ģ���ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
(1) һ���¶��£���һ���̶��ݻ����ܱ������У����淴Ӧ A(g) +2B(g)  4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��
4C (g) ��H >0 �ﵽƽ��ʱ��c(A) ="2" mol��L-1��c ( B) =" 7" mol��L-1��c ( C) =" 4" mol��L-1����ȷ��B����ʼŨ��c (B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� ��
A. ����C�����ʵ��� B. ��ѹ
C. ���� D.ʹ�ô���
��2�������£�ȡ pH=2������ʹ�����Һ��100mL, �����зֱ����������Zn������Ӧ����������Һ��pH�仯����ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ��� ( �A����B��)�� �������м����Zn����Ϊm1��������Һ�м����Zn����Ϊ m2�� ��
m1 m2 ( ѡ�<������=������>��)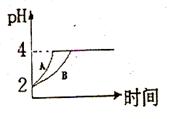
(3) �����Ϊ3L���ܱ������У�CO��H2��һ�������·�Ӧ���ɼ״���CO ( g) + 2H2( g) �� CH3OH(g) ��H= ��91kJ��mol-1����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK= �������¶ȣ�Kֵ (���������С�����䡱)��
(4) ���ܵ������ˮ��Һ��Ҳ�����ܽ�ƽ�⡣�ڳ����£���Һ�������Ũ�������ǻ�ѧ������Ϊ���εij˻���һ�����������ܶȻ����������磺 Cu(OH)2(s) Cu2+ (aq) + 2OH - ( aq)��Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2��10" -20������Һ�и�����Ũ�ȼ��������εij˻������ܶȻ�ʱ���������������ijCuSO4��Һ��c( Cu2+) ="0.02" mol��L-1���������Cu(OH)2������Ӧ������ҺpH��ʹpH���� �� Ҫʹ0.2 mol��L-1��CuSO4��Һ��Cu2+������Ϊ��ȫ ( ʹCu2+Ũ�Ƚ���ԭ�������֮һ)��Ӧ����Һ���NaOH��Һ��ʹ��ҺpH���� ��
Cu2+ (aq) + 2OH - ( aq)��Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2��10" -20������Һ�и�����Ũ�ȼ��������εij˻������ܶȻ�ʱ���������������ijCuSO4��Һ��c( Cu2+) ="0.02" mol��L-1���������Cu(OH)2������Ӧ������ҺpH��ʹpH���� �� Ҫʹ0.2 mol��L-1��CuSO4��Һ��Cu2+������Ϊ��ȫ ( ʹCu2+Ũ�Ƚ���ԭ�������֮һ)��Ӧ����Һ���NaOH��Һ��ʹ��ҺpH���� ��
(5) �����£�ij����(Na2CO3) ��Һ�е����̪����Һ�ʺ�ɫ�������Һ�� �ԡ��ڷ�������Һ����̪�ʺ�ɫԭ��ʱ����ͬѧ��Ϊ��������Һ���õĴ�����Ʒ�л���NaOH ���£���ͬѧ��Ϊ����Һ��Na2CO3�������CO32-ˮ�����¡��������һ����ʵ�鷽���������м�����λͬѧ�Ĺ۵��Ƿ���ȷ(��������������ͽ���) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ�����и߶���ѧ����ĩ���в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ���ס��ҡ����ֱ��ʾ�ڲ�ͬ�����£����淴ӦA(g)��B(g) xC(g)��������C�ڷ�Ӧ������еİٷֺ���w(C)�ͷ�Ӧʱ��(t)�Ĺ�ϵ������˵����ͼ����ϵ���
xC(g)��������C�ڷ�Ӧ������еİٷֺ���w(C)�ͷ�Ӧʱ��(t)�Ĺ�ϵ������˵����ͼ����ϵ���

A����ͼ��a��ʾ��Ӧ�ﵽƽ����ں��º�ѹ�����³��뺤��������
B����ͼ��b���߱�ʾ�д��������
C�����ݱ�ͼ�����жϸÿ��淴Ӧ������Ӧ�����ȷ�Ӧ�� x>2
D����ͼ�ɱ�ʾ��ij�̶��ݻ����ܱ������У��������淴Ӧ�ﵽƽ���A��������������¶�(T)�仯�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com